
在元素周期表中,相邻近的元素在结构和性质上有许多相似之处。
(1)第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H2O外,还有H2O2;碳元素的氢化物除CH4外,还有C2H6等;与之相似的氮元素的氢化物除NH3外,还有________(填化学式),其沸点比液氨____(填“高”或“低”),该氢化物与足量盐酸反应的化学方程式为______________________________。
(2)氮原子间也可形成链状结构,假设氮原子间只以N-N键形式连接,并形成氢化物,则该系列氢化物的通式为___________________。
(3) (2)题的通式中氮原子数是2的化合物和NO2混合发生反应生成N2和H2O(气),今知4 g该气态化合物在上述反应中放出71kJ热量,写出其热化学方程式为:
。由于该反应放出大量热,可作火箭推进剂,发射宇宙飞船。载人飞船内需要有一种化合物来吸收宇航员呼出的 CO2并提供O2,写出该物质的电子式________________。飞船中需要制造一种适合宇航员生存的人工生态环境,应该在氧气中充入一种气体用于稀释氧气,该气体分子的电子式是__________。
(14分,每空2分)(1)N2H4,高,N2H4+2HCl=N2H6Cl2 (2)NnHn+2
(3)2N2H4(g) + 2NO2 (g) = 3N2 (g) + 4H2O(g) ; △H = — 1136 kJ/ mol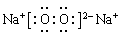
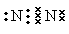
解析试题分析:(1)根据性质的递变规律可知,氮元素的氢化物除NH3外,还有N2H4。该化合物的相对分子质量大于氨气的,所以沸点高于液氨的。由于分子中含有2个氮原子,所以可以结合2分子氯化氢,即反应的化学方程式是N2H4+2HCl=N2H6Cl2。
(2)根据氨气和N2H4的结构可知,氨气的分子中比N2H4少2个氢原子、1个氮原子,所以该系列氢化物的通式为NnHn+2。
(3)通式中氮原子数是2的化合物是N2H4,由于4 g该气态化合物在上述反应中放出71kJ热量,则1mol该化合物反应放出的热量是71kJ×32/4=568kJ,所以该反应的热化学方程式是2N2H4(g) + 2NO2 (g) = 3N2 (g) + 4H2O(g) ; △H = — 1136 kJ/ mol。作为供氧剂的是过氧化钠,其电子式是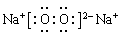 。适合宇航员生存的人工生态环境应该是空气,所以充入用于稀释氧气的气体应该是氮气,所以该气体分子的电子式是
。适合宇航员生存的人工生态环境应该是空气,所以充入用于稀释氧气的气体应该是氮气,所以该气体分子的电子式是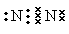 。
。
考点:考查物质结构和沸点的判断,电子式、热化学方程式、化学方程式书写
点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题基础性强,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和知识的迁移能力,也有助于培养学生的规范答题能力和应试能力。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 键能(kJ/mol) | 键能(kJ/mol) | 键能(kJ/mol) | |||
| H-H | 436 | C-Cl | 243 | H-Cl | 432 |
| Cl-Cl | 330 | C-I | 218 | C-F | 427 |
| C-O | 347 | H-O | 464 | H-F | 565 |
| 选项 | 现象:沸点H2O>H2S | 原理:键能H-O>H-S | 原理对现象的解释 |
| A | 正确 | 正确 | 可以 |
| B | 错误 | 正确 | |
| C | 正确 | 错误 | |
| D | 正确 | 正确 | 不可以 |
查看答案和解析>>
科目:高中化学 来源: 题型:




查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


 ,你认为
,你认为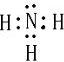
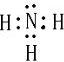
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com