
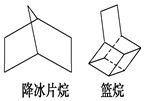
 如图都是简化的碳架结构:
如图都是简化的碳架结构:分析 (1)由结构及C形成4个共价键分析分子式;
(2)降冰片烷的结构对称,含3种H;
(3)由结构对称性可知,从上到下有4种位置的H.
解答 解:(1)由降冰片烷结构简式可知其分子中含有7个碳原子、12个氢原子,则分子式为为C7H12;篮烷的结构简式可知其分子中含有10个碳原子、12个氢原子,则分子式为为C10H12,故答案为:C7H12;C10H12;
(2)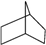 的结构对称,分子中含3种位置的H,则一氯取代时,取代位置有3种,故答案为:3;
的结构对称,分子中含3种位置的H,则一氯取代时,取代位置有3种,故答案为:3;
(3)结构对称,含4种位置的H,则其一氯代物有4种,故答案为:4.
点评 本题考查有机物的结构与性质,为高频考点,把握C形成的化学键及结构对称性为解答的关键,侧重分析与应用能力的考查,注意H种类的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CaO和KCl | B. | CuO和NaCl | C. | BaSO4和CaCO3 | D. | NaCl和AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
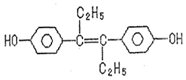
| A. | 可与NaOH和NaHCO3发生反应 | |
| B. | 可以用有机溶剂萃取 | |
| C. | 1mol该有机物可以与5molBr2发生反应 | |
| D. | 该有机物分子中,可能有18个碳原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AX | B. | BX | C. | AY | D. | BY |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL 2mol•L-1 KClO3溶液 | B. | 75mL 2mol•L-1CaCl2溶液 | ||
| C. | 150mL 2mol•L-1 KCl溶液 | D. | 75mL 1mol•L-1AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.20 | 0.10 | 0.09 | 0.08 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnS的Ksp比CuS的Ksp小 | |
| B. | 该反应达平衡时c(Mn2+)=c(Cu2+) | |
| C. | 设该反应的平衡常数为K,则该关系成立:K×Ksp(CuS)=Ksp(MnS) | |
| D. | 往平衡体系中加入少量CuSO4固体后,c(Cu2+)减小,c(Mn2+)变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁的硬度小于铝 | B. | 镁的熔、沸点低于钙 | ||
| C. | 镁的硬度大于钾 | D. | 钙的熔、沸点高于钾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com