
【题目】某研究性学习小组利用下面的装置自制Zn﹣O2燃料电池,步骤如下: 
Ⅰ.利用电解装置(如图1,A、B均为石墨棒),在多孔的石墨棒上吸附一定量的氧气.
Ⅱ.取出吸附有氧气的石墨棒,用导线将石墨棒、锌板和小灯泡连接,并将石墨棒和锌板插入KNO3溶液中,组装成Zn﹣O2燃料电池(如图2),使灯泡发光.
(1)电解水的装置中,产生氧气的电极是(填“A”或“B”).
(2)Zn﹣O2燃料电池正极的电极反应式是 , 该电池放电时溶液中的NO3﹣向极移动(填“正”或“负”).
(3)如果Zn﹣O2燃料电池的锌电极质量减少0.13g,那么电解池中产生氢气在标准状况下的体积至少为mL.
科目:高中化学 来源: 题型:
【题目】如图1所示的过程是目前直接利用太阳能的研究热点,人们把通过人工光化学手段合成燃料的过程叫做人工光合作用. 
(1)在如图构想的物质和能量循环中太阳能最终转化为能.
(2)图2中能表示甲烷燃烧过程中的能量变化的是(填序号).
(3)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH4 . 该反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHC2O4溶液的pH < 7。常温下,向pH=8.4的Na2C2O4溶液中滴加0.1mol/L的HCl溶液,溶液pH与pOH[pOH=-lgc(OH-)]的变化关系如图所示,下列各点所示溶液中微粒的物质的量浓度关系一定正确的是
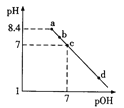
A. a点:c(H+)+c(HC2O4-)+2c(H2C2O4)=c(OH-)
B. b点:c(Cl-)>c(H2C2O4)+c(HC2O4-)+c(C2O42-)
C. c点:c(Na+)=c(HC2O4-)+ c(C2O42-)+c(Cl-)
D. d点:c(OH-)+ c(Cl-)=c(H+)+2c(H2C2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 常温下醋酸分子不可能存在于pH>7的碱性溶液中
B. 0.1 mol·L-1碳酸氢钠溶液中离子浓度关系是:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
C. 常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中:c(Cl-)>c(NH![]() )
)
D. 0.1 mol·L-1氯化铵溶液与0.1 mol·L-1的氢氧化钠溶液等体积混合溶液中的离子浓度为:c(Cl-) > c(Na+) > c(NH![]() ) > c(OH-)
) > c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃时,下列各种情况下一定能大量共存的离子组为( )
A. pH=2的溶液中:Fe2+、Cl-、Na+、NO![]()
B. 由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、CO![]() 、Cl-、K+
、Cl-、K+
C. 在能使石蕊试液变红的溶液中:NH![]() 、Cl-、Mg2+、SO
、Cl-、Mg2+、SO![]()
D. 在某无色溶液中:Fe3+、HCO![]() 、SO42-、Na+
、SO42-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液、胶体和浊液这三种分散系的根本区别是( )
A. 是否有丁达尔现象 B. 是否均一、透明、稳定
C. 分散质粒子直径的大小 D. 是否能通过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾的化学式可表示为FeSO4·xH2O,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的某些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加少量稀H2SO4后,再滴加KSCN溶液,溶液颜色无明显变化。充分振荡后,溶液逐渐变红。溶液变红的原因是_________(用离子方程式表示)。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。

①下列实验操作步骤的正确排序为___________________(填标号);重复上述操作步骤,直至A恒重,记为m3g。
a.关闭K1和K2 b.打开K1和K2,缓缓通入N2 c.点燃酒精灯,加热 d.称量A e.冷却到室温 f.熄灭酒精灯
②判断A是否恒重的方法是____________________。
③根据实验记录,绿矾化学式中结晶水数目x=________________(列式表示)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入由下图所示仪器组装而成的装置中,打开K1和K2,缓缓通入N2一段时间后,加热。实验后反应管中残留固体为红色粉末。
①反应中有两种气体产物生成,为检验该气体混合物的组成,请从下图所示的仪器中,选择合适的仪器(含其中的试剂),组成一套实验装置,该装置的连接顺序(按气体流向从左到右)依次为___________→D(填装置序号)。装置中除有气泡冒出外,其他证明实验结论的现象分别为__________________________。

②硫酸亚铁高温分解的化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度。有关的叙述中,正确的是
A. H2Y电离方程式为:H2Y+H2O![]() HY-+H3O+
HY-+H3O+
B. 常温下,该酸式盐的水溶液中溶液中,各离子浓度大小关系为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C. 常温下,酸式盐NaHY 的水溶液呈酸性
D. HY-的水解方程式为:HY-+ H2O![]() H3O++Y2-
H3O++Y2-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com