
将氯气通入含有下列大量离子的各组溶液中,无明显现象的是( B )
A. H+、Ag+、NO![]() B. Na+、OH-、Cl-
B. Na+、OH-、Cl-
C. K+、HCO![]() 、NO
、NO![]() D. K+、SO
D. K+、SO![]() 、Bl-
、Bl-
【解析】 A会生成氯化银的沉淀;C会产生二氧化碳气体;D会生成溴单质而出现颜色;B虽然会与氯气反应,但无明显现象。故选B。
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
13 6 |
39 19 |
40 20 |
12 6 |
14 7 |
40 18 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| n(ClO-) | n(ClO3-) |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
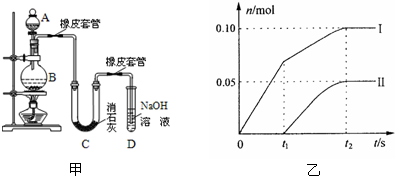
查看答案和解析>>
科目:高中化学 来源: 题型:
| 提出问题 | 收集资料 | 提出假设 | 验证假设 | 得出结论 |
| 氯水中何种物质能使湿润的红色布条褪色 | ①氯气有强氧化性 ②氯气与冷水反应生成盐酸和次氯酸 ③次氯酸有强氧化性 |
① ② ③ ④H2O使布条褪色 |
实验①:把红色干布条放入充满氯气的集气瓶中,布条不褪色 实验②: 实验③: 实验④:把红色布条放在水里布条不褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com