
等质量的氯气与下列足量物质反应,转移的电子数最少的是( )
|
| A. | 冷的NaOH溶液 | B. | SO2的水溶液 | C. | FeCl2溶液 | D. | 铜 |
| 化学方程式的有关计算.. | |
| 分析: | 根据氯气和选项中物质反应的过程中,氯元素的化合价升降情况确定转移电子数目,得到结果即可. |
| 解答: | 解:等质量的氯气与足量物质反应,假设氯气中的质量都是71g,即1mol, A、1mol氯气和氢氧化钠反应生成氯化钠和次氯酸钠,转移电子是1mol; B、1mol氯气和SO2的水溶液反应生成盐酸和硫酸,转移电子是2mol; C、1mol氯气和FeCl2的水溶液反应生成氯化铁溶液,转移电子是2mol; D、1mol氯气和Cu反应生成氯化铜,转移电子是2mol; 转移的电子数最少的是A. 故选A. |
| 点评: | 本题考查学生化学方程式中的电子转移的计算知识,注意氧化还原反应知识的灵活应用,难度中等. |


科目:高中化学 来源: 题型:
 下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。
下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | a | |||||||
| 2 | b | c | d | |||||
| 3 | e | g | f |
(1)a元素和c元素可以形成的气体,其化学式为 ;
(2)e的元素符号是 ;
(3)b元素原子的最外层电子数为 ;
(4)b、c、d三种元素的非金属性逐渐 (填“减弱”或“增强”);
(5)d元素和f元素均可形成气态氢化物,其稳定性为H2d H2f (填“大于”或“小于”)。
(6)上述七种元素的最高价氧化物的水合物中,碱性最强的是 ,酸性最强的是 ,既有酸性又有碱性的是 (写化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列化学反应方程式:
(1)用乙烯制备聚乙烯: ;
反应类型 。
(2)2-氯丙烷与NaOH的水溶液共热: ;
反应类型 。
实验室制溴苯: ;
反应类型 。
(4)甲苯与浓硝酸和浓硫酸混合液共热生成三硝基甲苯:
;反应类型 。
(5)1,3-二溴-2,3-二甲基丁烷与NaOH的醇溶液共热:
;反应类型 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将1mol SO2和1mol O2通入一体积不变的密闭容器中,在一定温度和催化剂作用下,反应达到平衡,SO3为0.3mol。此时若移走0.5mol O2和0.5mol SO2,则反应达到新的平衡时,SO3的物质的量为
A.小于0.15mol B.0.15mol
C.0.3mol D.大于0.15mol,小于0.3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景。
(1)工业生产甲醇的常用方法是:CO(g)+2H2(g)  CH3OH(g) △H=-90.8 kJ/mol ①
CH3OH(g) △H=-90.8 kJ/mol ①
已知:2H2(g)+ O2(g)= 2H2O (l) △H=-571.6 kJ/mol ②
H2(g) +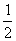 O2(g) = H2O(g) △H=-241.8 kJ/mol ③
O2(g) = H2O(g) △H=-241.8 kJ/mol ③
①H2的燃烧热为 ▲ kJ/mol。
②CH3OH(g)+O2(g)  CO(g)+2H2O(g)的反应热△H= ▲ kJ/mol。
CO(g)+2H2O(g)的反应热△H= ▲ kJ/mol。
③若在恒温恒容的容器内进行反应CO(g)+2H2(g)  CH3OH(g),则可用来判断该反应达到平衡状态的标志有 ▲ 。(填字母)
CH3OH(g),则可用来判断该反应达到平衡状态的标志有 ▲ 。(填字母)
A.CO百分含量保持不变 B.容器中H2浓度与CO浓度相等
C.容器中混合气体的密度保持不变 D.H2的生成速率与CH3OH的生成速率相等
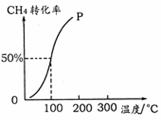 (2)将1.0 mol CH4和2.0 mol H2O ( g )通入容积为100 L的反应室,在一定条件下发生反应:CH4 ( g ) + H2O ( g ) =CO ( g ) + 3H2 ( g ) ,测得在一定的压强下CH4的转化率与温度的关系如右图。
(2)将1.0 mol CH4和2.0 mol H2O ( g )通入容积为100 L的反应室,在一定条件下发生反应:CH4 ( g ) + H2O ( g ) =CO ( g ) + 3H2 ( g ) ,测得在一定的压强下CH4的转化率与温度的关系如右图。
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为 ▲ 。
②100℃时反应I的平衡常数为 ▲ 。
(3)工业上利用甲醇制备氢气的常用方法有两种:
①甲醇蒸汽重整法。该法中的一个主要反应为CH3OH(g)  CO(g)+2H2(g),此反应能自发进行的原因是 ▲ 。
CO(g)+2H2(g),此反应能自发进行的原因是 ▲ 。
②甲醇部分氧化法。在一定温度下以Ag/CeO2—ZnO为催化剂时原料气比例对反应的选择性(选择性越大,表示生成的该物质越多)影响关系如图所示。

则当n(O2)/n(CH3OH)=0.25时,CH3OH与O2发生的主要反应方程式为
▲ ;
在制备H2时最好控制n(O2)/n(CH3OH)= ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸晶体的组成可表示为H2C2O4•xH2O.实验室常用其加热分解制取CO气体,反应方程式为:H2C2O4•xH2O  CO+CO2+(x+1)H2O.下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题.
CO+CO2+(x+1)H2O.下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题.
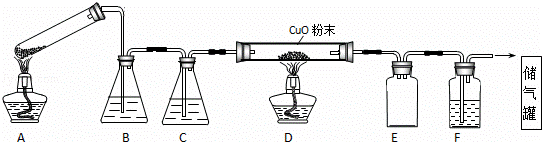
(1)A装置为加热分解草酸的装置,该装置错误是 试管口应向上倾斜(或应向下倾斜) ,C装置中盛放的试剂是 浓硫酸 (填化学式),E装置的作用是 安全瓶(或防倒吸) .
(2)实验过程中涉及到如下操作:①点燃A处的酒精灯 ②熄灭A处的酒精灯 ③点燃D处的酒精灯 ④熄灭D处的酒精灯.这4步操作由先到后的顺序为 ①③④② (填序号).点燃D处酒精灯前必须要进行的操作名称是 验纯 .
(3)用酸性高锰酸钾溶液滴定草酸晶体,求x的值.
实验步骤:准确称取1.17g 草酸晶体,配成100mL溶液;取出20.00mL于锥形瓶中,再向瓶中加入足量稀H2SO4;用0.0500mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液16.00mL.滴定时,所发生的反应为:2MnO4﹣+5H2C2O4+6H+=10CO2+2Mn2++8H2O.
①配制草酸溶液除需要玻璃棒、烧杯,还一定需要的玻璃仪器有 100mL容量瓶、胶头滴管 .
②x= 1.5 .
(4)为探究催化剂对化学反应速率的影响,在甲乙试管中分别加入下列物质
| 试管 | 0.01mol/L KMnO4 | 0.1mol/L H2C2O4 | 0.1mol/L H2SO4 | MnSO4固体 |
| 甲 | 4mL | x mL | 1mL | 无 |
| 乙 | y mL | 2mL | 1mL | 有 |
则x= 2 ,y= 4 .能够得出催化剂对该反应有影响结论的实验现象是 加入MnSO4固体的试管中溶液褪色速率比未加的快 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组元素的性质递变情况错误的是 ( )
A.Li、C、O原子最外层电子数依次增加
B.P、S、Cl元素最高正化合价依次升高
C.N、O、F原子半径依次增大
D.Li、Na、K的金属性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
根据所学知识回答下列问题,在如图所示装置中
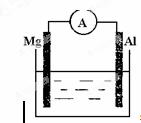 ,
,
(1)若烧杯中溶液为稀硫酸,则观察到的现象为 ,正极反应式为 ,负极反应式为 ,
该装置中的能量变化形式为 。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
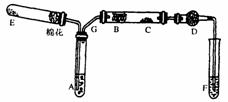 下图为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液。
下图为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液。
请回答下列问题:
(1) 如图所示连接好装置后,在加入试剂之前,应先 ____ 。(操作名称)
(2)在上述装置中,实验时需要加热的仪器为(填仪器或某部位的代号) 。
为使A中乙醇平缓均匀的气化成乙醇蒸气,常采用的操作方法是 。
(3)图中D处使用碱石灰的作用是 。
(4)C处观察到的现象是 ,
F中观察到的现象是 ,
说明B处发生的反应方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com