
| A. | 青蒿素的一个分子中含有42个原子 | |
| B. | 青蒿素属于无机物 | |
| C. | 青蒿素的相对分子质量为282 | |
| D. | 青蒿素中碳元素的质量分数约为63.8% |
分析 A.根据分子结构来分析;
B.根据有机物与无机物的判断方法来分析;
C.根据相对分子质量的计算方法来分析;
D.根据化合物中元素质量分数的计算方法来分析.
解答 解:A.由青蒿素的化学式可知,每个青蒿素分子中含有15个碳原子、22个氢原子和5个氧原子,共42个原子,故A正确;
B.由青蒿素的化学式可知,青蒿素是一种含碳元素的化合物,属于有机物,故B错误;
C.青蒿素的相对分子质量为12×15+1×22+16×5=282,故C正确;
D.青蒿素中碳元素的质量分数为$\frac{12×15}{282}$×100%≈63.8%,故D正确.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | 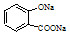 溶液通入少量CO2: 溶液通入少量CO2: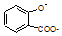 +CO2+H2O═ +CO2+H2O═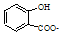 +HCO3- +HCO3- | |
| B. | 水电离产生的c(H+)=10-12mol•L-1的溶液中:Na+、Fe2+、SO42-、NO3-可能会大量共存 | |
| C. | 少量SO2通入NaClO溶液中:SO2+ClO-+OH-=SO42-+Cl-+H+ | |
| D. | 5.6 g Fe与200 mL 2.0 mol/L HNO3溶液:3Fe+2NO3-+8H+=3Fe2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 制备银氨溶液:向2%的氨水中逐滴加入足量的2%的AgNO3溶液 | |
| B. | 除去MgCl2溶液中少量FeCl3:向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌,充分反应后过滤 | |
| C. | 比较Ag2CO3与AgCl溶度积大小:向浓度均为0.1mol•L-1的Na2CO3和NaCl的混合溶液中滴加0.1mol•L-1 AgNO3溶液,观察现象 | |
| D. | 验证Fe3+与I-的反应有一定限度:向5mL0.1mol•L-1KI溶液中滴入0.1mol•L-1FeCl3溶液5~6滴,加2mLCCl4振荡,静置后取上层清液滴加KSCN溶液,观察现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)/c(OH?)=1的无色溶液中:Fe3+、NH4+、Cl?、SO42? | |
| B. | 使甲基橙呈黄色的溶液中:Na+、ClO?、SO42?、I? | |
| C. | 0.1 mol•L-1NaAlO2溶液:H+、Na+、Cl-、SO42- | |
| D. | pH=12的溶液:K+、Na+、CH3COO-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
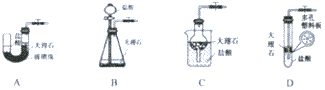
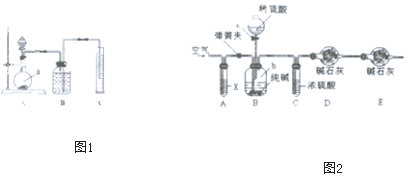
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒精和水.酒精和乙醚.溴苯和水 | |
| B. | 溴乙烷和水.乙酸乙酯和水.溴苯和水 | |
| C. | 溴苯和水.油脂和苯.蔗糖和葡萄糖 | |
| D. | 甘油和水.乙醛和水.乙酸和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ca2+、Cl-、SO42- | B. | Fe2+ H+ SO42- HCO3- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、NH4+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜电极电解CuSO4溶液 阳极:Cu-2e-=Cu2+ | |
| B. | 电镀铜时(电解质溶液为CuSO4溶液) 阳极:Cu2++2e-=Cu | |
| C. | 电解熔融NaCl 阴极:Na++e-=Na | |
| D. | 电解NaOH溶液 阳极:4OH--4e-=2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 硅、锗都位于金属与非金属的交界处,都可以做半导体材料 | |
| B. | 氢化物的沸点:H2O>NH3>HF | |
| C. | 同主族元素从上到下,单质的熔点逐渐降低 | |
| D. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com