
下列说法正确的是( )
A.在一定条件下,乙烯能与H2发生加成反应,苯不能与H2发生加成反应
B.C2H6O和C4H10都有2种同分异构体
C.乙酸乙酯、乙酸均能与NaOH反应,二者分子中官能团相同
D.淀粉和蛋白质均可水解生成葡萄糖
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
下列溶液或浊液中,关于离子浓度的说法正确的是
A.一定浓度的氨水加水稀释的过程中,c(NH4+)/ c(NH3·H2O)的比值减小
B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液中:
c(CO32-) > c(HCO3-),且2c(Na+)=3[c(CO32-)+c(HCO3-)]
C.0.2 mol·L-1的醋酸(CH3COOH)溶液与0.1 mol·L-1 NaOH溶液等体积混合后:
c(CH3COO-) + 2c(OH-) = c(CH3COOH) + 2c(H+)
D.常温下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2CrO4悬浊
液中的c(Ag+)一定小于AgCl悬浊液中的c(Ag+)
查看答案和解析>>
科目:高中化学 来源: 题型:
CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。
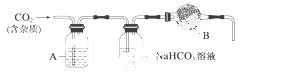
完成下列填空:
(1)用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol·L-1),应选用的仪器是_________。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
(2)上述装置中,A是____________,NaHCO3溶液可以吸收________。
(3)上述装置中,B物质是__________。用这个实验得到的气体测定CO2的分子量,如果B物质失效,测定结果________(填“偏高”、“偏低”或“不受影响”)。
(4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
为了将石蜡和碳酸钙溶出,应选用的试剂是__________。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸 d.正己烷
(5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出________,后溶出_______。
(6)上述测定实验中,连续__________,说明样品已经恒重。
查看答案和解析>>
科目:高中化学 来源: 题型:
贝诺酯是由阿司匹林、扑热息痛经化学法拼合制备的解热镇痛抗炎药,其合成反应式 (反应条件略去)如下:
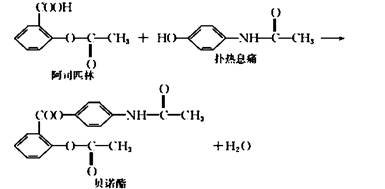
下列叙述错误的是
A. FeCl3溶液可区别阿司匹林和扑热息痛
B.1 mol贝诺酯最多可消耗3 mol NaOH
C.常温下,贝诺酯在水中的溶解度小于扑热息痛
D.与阿司匹林互为同分异构体,且1 mol能与足最NaHCO3溶液反应产生2mo1CO2的结构为10种
查看答案和解析>>
科目:高中化学 来源: 题型:
今年国际化学年的主题是“化学—我们的生活,我们的未来”。下列说法不正确的是 ( )
A.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。PM2.5被吸入人体后会直接进入支气管,易引发包括哮喘、支气管炎和心血管病等方面的疾病
B.高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路”
C.利用二氧化碳等原料合成的聚碳酸酯类可降解塑料替代聚乙烯塑料
D.生物柴油的主要成分是利用从泔水中提取的地沟油与甲醇反应生成的脂肪酸甲酯类化合物,与石化柴油有本质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
关于氯化钠、氯化钙、氯化钾的下列说法正确的是( )
A.工业上利用钠与氯气反应制取氯化钠
B.向氯化钠的饱和溶液中加入少量钠无明显现象
C.氯化钙是漂白粉的有效成分
D.向氯化钠、氯化钙、氯化钾的溶液中分别加入少量硝酸银溶液,均出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为___________________。
(2)漂白粉的有效成分是(填名称)________。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,反应的离子方程式为______________________________。
(4)反应(1)和反应(3)中,属于氧化还原反应的是(填编号)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示是验证氯气性质的 微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl—→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是 ( )
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
研究下表信息可直接得出的结论是 ( )
| 元素 | F | Cl | Br | I |
| 氢化物组成 | HF | HCl | HBr | HI |
| 氢化物形成难 易程度 | H2、F2混合,冷暗处剧烈化合并发生爆炸 | H2、Cl2混合,光照或点燃时发生爆炸 |
| H2、I2混合,加热化合,同时又分解 |
| 氢化物热稳定性 | 很稳定 | 稳定 | 较稳定 | 较不稳定 |
A.元素性 质随原子序数的递增而呈周期性变化
质随原子序数的递增而呈周期性变化
B.同周期元素的非金属性随原子序数递增而增强
C.第ⅦA族元素的金属性随电子层数增加而减弱
D.第ⅦA族元素的非金属性随电子层数增加而减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com