

| A£®NaCl”¢Cl2 | B£®NaCl”¢NaClO | C£®NaClO3”¢NaClO4 | D£®NaCl”¢NaClO3 |
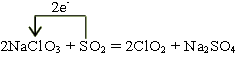 ----------------3·Ö
----------------3·Ö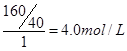 ”£
ӣ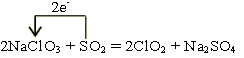 ӣ
ӣ

 æŖŠÄĶÜדŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
æŖŠÄĶÜדŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®NH4CuSO3ÖŠĮņŌŖĖŲ±»Ńõ»Æ | B£®øĆ·“Ó¦±ķĆ÷ĮņĖį¾ßÓŠĖįŠŌ |
| C£®“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢåŹĒ°±Ęų | D£®øĆ·“Ó¦ÖŠĮņĖį×÷Ńõ»Æ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®·“Ӧɜ³ÉĪļ¶¼ŹōÓŚµē½āÖŹ | B£®øĆ·“Ó¦±ķĆ÷Ńõ»ÆŠŌCl2±ČKClO3Ēæ |
| C£®HCl²æ·Ö·¢ÉśŃõ»Æ·“Ó¦ | D£®1mol KClO3ŌŚ·“Ó¦ÖŠµĆµ½6mole£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Br2ŌŚ·“Ó¦ÖŠ±ķĻÖŃõ»ÆŠŌ | B£®SO2ŌŚ·“Ó¦ÖŠ±»»¹Ō |
| C£®Br2ŌŚ·“Ó¦ÖŠŹ§Č„µē×Ó | D£®1 molŃõ»Æ¼ĮŌŚ·“Ó¦ÖŠµĆµ½1 molµē×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Cu2S Ö»×ö»¹Ō¼Į | B£®O2·¢ÉśŃõ»Æ·“Ó¦ |
| C£®SŌŖĖŲ±»Ńõ»Æ | D£®µ±0.8mol O2²Ī¼Ó·“Ó¦Ź±£¬¹²×ŖŅĘĮĖ3.2molµē×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¢Ł¢Ū¢Ü | B£®¢ŪI2¢ß | C£®¢Ū¢Ż | D£®¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| A£®¼×ŗĶ±ūÖŠĶ¬ÖÖŌŖĖŲ»ÆŗĻ¼Ū²»æÉÄÜĻąµČ |
| B£®øĆ·“Ó¦ŹōÓŚŃõ»Æ»¹Ō·“Ó¦ |
| C£®¶”ĪļÖŹŅ»¶ØŹĒ·Ē½šŹōµ„ÖŹ |
| D£®ÅäĘ½ŗó¼×”¢ŅŅ”¢±ūµÄ»Æѧ¼ĘĮæŹż¾łĪŖ2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com