
【题目】已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑,A和X反应的转化关系如下图所示,其中反应条件及部分产物均已略去,下列有关说法正确的是( )

A.X能使蔗糖变黑主要体现了X的强氧化性
B.若A为铁,则足量A与X在室温下即可完全反应
C.若A为碳单质,则将C通入少量的澄清石灰水中,最终一定有白色沉淀产生
D.工业上,B转化为D的反应需使用催化剂
科目:高中化学 来源: 题型:
【题目】下列叙述中与氮的固定无关的是
A.工业合成氨
B.工业上将氨转化成硝酸和其他氮的氧化物
C.豆科植物的根瘤菌吸收空气中的氮气使之转化成植物蛋白质
D.电闪雷鸣的雨天,N2与O2会反应并最终转化为硝酸盐被植物吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近来, 科学家研制了一种新型的乙醇电池(DEFC), 它用磺酸类质子作溶剂, 在200℃左右时供电, 乙醇电池比甲醇电池效率高出32倍且更加安全。电池总反应式为: C2H5OH+3O2 ![]() 2CO2+3H2O。下列说法不正确的是
2CO2+3H2O。下列说法不正确的是
A.C2H5OH在电池的负极上参加反应 B.1 mol乙醇被氧化转移6 mol电子
C.在外电路中电子由负极沿导线流向正极 D.电池正极得电子的物质是O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2与SO3(g)的反应类似于Na2O2与CO2(g)的反应,请写出Na2O2与SO3反应的化学方程式: . 每2molNa2O2参加反应,转移电子数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A.
光解水的催化材料可用硝酸镍、硫脲和锐钛矿为原料,采用醇热法制得。
(1)Ni2+基态核外电子排布式为__________________。
(2)与NO3-互为等电子体的一种分子的化学式为__________________。
(3)硫脲(![]() )中C原子轨道的杂化类型为__________________;
)中C原子轨道的杂化类型为__________________;
1 mol硫脲中含有键的数目为____________mol。
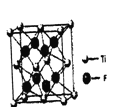
钛的一种氟化物晶胞结构如右图所示,其化学式为____________。
(5)甘油(丙三醇)具有保持水分的功效,其主要原因是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止人们已发现或合成了118种元素,元素①~⑨在周期表中的位置如下表所示(序号代表对应的元素)。
① | |||||||||||||||||
② | ③ | ④ | ⑤ | ||||||||||||||
⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||||
…… | |||||||||||||||||
(1)④在周期表中位于第___________周期___________族。
(2)9种元素中原子半径最大的是___________(填元素符号),非金属性最强的是___________(填元素符号);
(3)最高价氧化物的水化物的碱性⑥___________⑦(填“>”或“<”)。
(4)⑧的阴离子的结构示意图为___________;③的简单氢化物与⑨的最高价氧化物的水化物化合生成的盐的化学式为___________。
(5)能说明⑨的非金属性比③强的化学方程式为___________。
(6)1971年在星际空间发现一种由①、②、③三种元素组成的直线型有机分子X。X的摩尔质量为51g·mol-1,且X分子中共含5个原子(各原子均满足稀有气体原子的稳定结构),X的结构式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com