
【化学—选修3物质结构与性质】(15分)
(1) A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(KJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
根据上述信息,写出B的基态原子核外电子排布式 ,预测A和氯元素形成的简单分子空间构型为 。
(2)钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,往其中一种配合物的溶液中加入AgNO3溶液时,无明显现象,往其溶液中加BaCl2溶液时若,产生白色沉淀,则该配合物的化学式为 ,中心离子的配位数为 。
(3)参考下表中的物质熔点回答下列问题
| 物质 | NaF | NaCl | NaBr | NaI | NaCl | KCl | RbCl | CsCl |
| 熔点(℃) | 995 | 801 | 755 | 651 | 801 | 776 | 715 | 646 |
根据上表数据解释钠的卤化物及碱金属的氯化物的熔点变化规律 。
(4) C60可用作储氢材料。C60的结构如图1。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确 ,并阐述理由 。科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体,该物质的K原子和C60分子的个数比为 。
(5)三聚氰胺分子的结构简式如图3,则其中氮原子轨道杂化类型是 ,l mol三聚氰胺分子中含 mol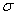 键。
键。
(6)碳化硅的晶胞与金刚石的晶胞相似如图4,设晶胞边长为a cm,碳原子直径为b cm,硅原子直径为c cm,则该晶胞的空间利用率为 (用含a、b、c的式子表示)。
科目:高中化学 来源: 题型:
某有机物分子结构如下:

关于该分子结构的说法正确的是( )
A.除苯环外的其余碳原子有可能都在一条直线上
B.除苯环外的其余碳原子不可能都在一条直线上
C.12个碳原子不可能都在同一平面上
D.12个碳原子一定都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
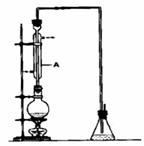
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应.某课外小组欲在实验室制备溴乙烷的装置如右图,实验操怍步骤如下:
 ①检查装置的气密性; ②在圆底烧瓶中加入95%乙醇、溴化钠、浓硫酸及几粒碎瓷片;
①检查装置的气密性; ②在圆底烧瓶中加入95%乙醇、溴化钠、浓硫酸及几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是 。
(2)反应结束后,得到的粗产品呈棕黄色(含少量的溴单质)。为
了除去粗产品中的杂质,可选择下列试剂中的
(填写上正确选项的字母)。
a.亚硫酸钠溶液 b.氢氧化钠溶液
c.乙醇 d.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称)。
(3)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水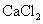 ,然后进行的实验操作是 (填写正确选项的字母)。
,然后进行的实验操作是 (填写正确选项的字母)。
a.分液 b.蒸馏 c.萃取
(4)为了检验溴乙烷中含有溴元素,通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号)。
①加热 ②加入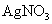 溶液 ③加入稀
溶液 ③加入稀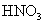 酸化 ④加入Na OH溶液
酸化 ④加入Na OH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
隔膜电解法处理高浓度乙醛废水的原理是使乙醛分别在两极发生反应,转化为乙醇和乙酸。实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液, 模拟乙醛废水的处理过程,其装置示意图如右图所示。有关说法不正确的是
A.图中燃料电池的a极应通入氧气
B.乙醇在阴极产生
C.电解过程中,阴极区有NaOH产生
D.每生成1mol乙酸,理论上至少消耗标况下氧气22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于碱金属的电子结构和性质的叙述中不正确的是( )
A.碱金属原子最外层都只有一个电子,在化学反应中容易失去 B.都是强还原剂
C.都能在O2中燃烧生成过氧化物 D.都能与水反应生成碱
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室常用邻苯二甲酸氢钾(KHC8H4O4)来滴定氢氧化钠的的浓度,反应如下:KHC8H4O4 + NaOH = KNaC8H4O4 + H2O。若氢氧化钠的溶液浓度为0. 1mol·L-1,到达终点时,溶液的PH约为9.1.
(1)为标定氢氧化钠溶液的浓度,应选 用作指示剂,达到滴定终点时溶液由
色变为 色。
(2)在测定氢氧化钠溶液浓度时,有下列操作:①向溶液中加入1-2滴指示剂 ②向锥形瓶中加20-30ml蒸馏水溶解 ③用氢氧化钠溶液滴定到终点,半分钟不褪色④重复以上操作 ⑤准确称取0.4-0.5g邻苯二甲酸氢钾加入250ml锥形瓶中⑥根据两次实验数据计算氢氧化钠的物质的量浓度。
以上各步中,正确的(填序号)操作顺序是
(3)上述操作中,将邻苯二甲酸氢钾直接放到锥形瓶中溶解,对实验是否有影响?
并说明理由: 

(4)滴定前,用蒸馏水洗净碱式滴定管,然后加待测定的氢氧化钠溶液滴定,此操作对实验结果 (填“偏大”“偏小”或“无影响”)
(5)现准确称取KHC8H4O4(分子量204.2)晶体0.5105g,溶于水后加入指示剂,用NaOH溶液滴定至终点,消耗NaOH 20 mL,则NaOH溶液的浓度为 (结果保留四位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com