
| 物质 | Fe(OH)2 | Fe(OH)3 |
| Ksp/25 ℃ | 2.0×10-16 | 4.0×10-36 |
 BCD
BCD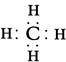
 Fe(OH)2↓+2Fe(OH)3↓+8NH4+
Fe(OH)2↓+2Fe(OH)3↓+8NH4+ ;由气态氢化物的沸点无法确定元素的非金属性强弱。答案选BCD。
;由气态氢化物的沸点无法确定元素的非金属性强弱。答案选BCD。 。
。 Fe(OH)2↓+2Fe(OH)3↓+8NH4+。
Fe(OH)2↓+2Fe(OH)3↓+8NH4+。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.钠久置于空气中,可以和空气中的有关物质反应,最终生成NaHCO3 |
| B.在高温下用氢气还原MgCl2可制取金属镁 |
| C.实验测得NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3 COOH>H2CO3 |
| D.氮气的化学性质通常非常稳定,但在放电条件下可以与O2反应生成NO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某无色溶液中滴加BaCl2溶液出现白色沉淀,说明该无色溶液中一定含有SO42— |
| B.向2.0 mL浓度均为0.1 mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01 mol·L-1AgNO3溶液,振荡,生成黄色沉淀,说明Ksp(AgI)比Ksp(AgCl)大 |
| C.铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜熔点高于铝 |
| D.SO2、Cl2都能使品红试液褪色,其原理是相同的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯气可以使湿润的有色布条褪色,是因为氯气具有漂白性 |
| B.用氢氟酸雕刻玻璃,是由于氢氟酸能与二氧化硅反应 |
| C.向50 mL 18 mol·L-1的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量等于0.45 mol |
| D.常温下,浓硝酸可以用铝制容器贮存,说明铝与浓硝酸不反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B.Na2O2、K2O2可用作潜水艇内的氧气来源 |
| C.Al2O3的熔点很高,可用于制作耐高温材料 |
| D.电解MgCl2饱和溶液,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 操 作 | 现 象 | 解释、结论 |
| A | 过量的Fe粉中加入硝酸充分反应,滴入KSCN溶液 | 溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | Al箔插入稀硝酸中 | 无现象 | Al箔表面被硝酸氧化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
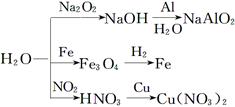
| A.如图所示的反应均为氧化还原反应 |
| B.比较镁、铁与水的反应条件,可知铁的金属性比镁弱 |
| C.工业上常用NO2与水的反应原理制取硝酸 |
| D.实验室中可用铜与稀硝酸反应制取NO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com