
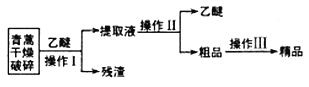
【题目】青蒿素是一种有效的抗疟药。常温下,青蒿素为无色针状晶体,难溶于水,易溶于有机溶剂,熔点为156~157℃。提取青蒿素的方法之一是乙醚浸取法,提取流程如下:
请回答下列问题:
(l)对青蒿进行破碎的目的是__________________。
(2)操作I用到的玻璃仪器是__________,操作Ⅱ的名称是_______。
(3)用下列实验装置测定青蒿素的化学式,将28.2g青蒿素放在燃烧管C中充分燃烧:
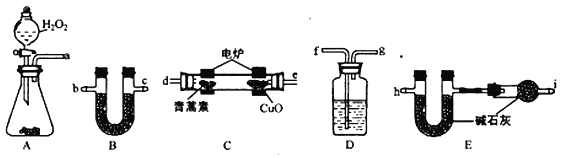
① 仪器各接口的连接顺序从左到右依次为_______(每个装置限用一次)。A装置中发生的化学反应方程式为_________________。
② 装置C中CuO的作用是_________________。
③ 装置D中的试剂为_________________。
④ 已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验.测量数据如下表:
装置质量 | 实验前/g | 实验后/g |
B | 22.6 | 42.4 |
E(不含干燥管) | 80.2 | 146.2 |
则青蒿素的最简式为__________。
(4)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH 、酚酞的水溶液中,青蒿素的溶解度较小,加热并搅拌,青蒿素的溶解度增大,且溶液红色变浅,与青蒿素化学性质相似的物质是______(填字母代号)。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
【答案】 增大青蒿与乙醚的接触面积,提高青蒿素的浸取率 漏斗、玻璃棒、烧杯 蒸馏 afgdebchi 2 H2O2 ![]() 2 H2O+O2 使青蒿素充分氧化生成CO2和H2O 浓硫酸 C15H22O5 C
2 H2O+O2 使青蒿素充分氧化生成CO2和H2O 浓硫酸 C15H22O5 C
【解析】本题分析:本题主要考查物质的分离方法。
(l)对青蒿进行破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率。
(2)操作I是过滤,用到的玻璃仪器是漏斗、玻璃棒、烧杯,操作Ⅱ将乙醚溶液中的乙醚分离出来,其名称是蒸馏。
(3)① 装置A产生的氧气需要经过装置D干燥,纯净的氧气进入装置C,产生的水蒸气被装置B吸收,二氧化碳被装置E吸收,仪器各接口的连接顺序从左到右依次为afgdebchi。A装置中发生反应的化学方程式为2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。
② 装置C中CuO的作用是使青蒿素充分氧化生成CO2和H2O。
③ 装置D中的试剂为干燥剂浓硫酸。
④B吸收水19.8g,其中含氢2.2mol即2.2g,E吸收二氧化碳66g,其中含碳1.5mol即18g,28.2g青蒿素含氧8g即0.5mol,则青蒿素的最简式为C15H22O5。
(4)在含有NaOH 、酚酞的水溶液中,乙酸乙酯水解,生成物乙酸与氢氧化钠反应使溶液红色变浅,所以与青蒿素化学性质相似的物质是乙酸乙酯,故选C。


 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】近年科学家提出“绿色自由”构想。把含有大量CO2的空气吹入K2CO3溶液中,再把CO2从溶液中提取出来,并使之与H2反应生成可再生能源甲醇。其工艺流程如图所示:
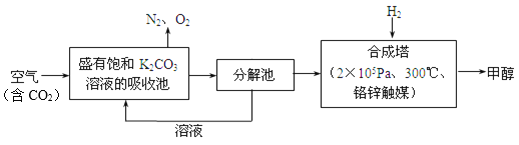
(1)分解池中主要物质是_______________。
(2)在合成塔中,若有4400 g CO2与足量H2反应,生成气态的H2O和甲醇,可放出5370 kJ的热量,写出该反应的热化学方程式_______________。
(3)该工艺在哪些方面体现了“绿色自由”构想中的“绿色”_______________。
(4)一定条件下,往2L恒容密闭容器中充入1 mol CO2和3 mol H2,在不同催化剂作用下发生反应I、反应II与反应III,相同时间内CO2的转化率随温度变化如下图所示:
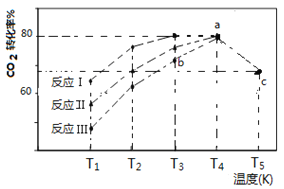
(图中c点的转化率为66.67%,即转化了2/3)
①催化剂效果最佳的反应是________(填“反应I”,“反应II”,“反应III”)。
②b点v (正)_________v (逆)(填 “>”, “<”, “=”)。
③若此反应在a点时已达平衡状态,a点的转化率比c点高的原因是____________。
④c点时该反应的平衡常数K =____________________。
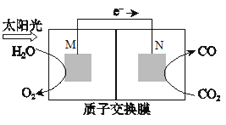
(5)科学家还研究了其它转化温室气体的方法,利用下图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N电极的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知,有机化合物A只由碳、氢两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化工发展水平。A、B、C、D、E有如下关系:

则下列推断不正确的是 ( )
A. 鉴别A和甲烷可选择使用酸性高锰酸钾溶液
B. B中含有的官能团为羟基,B物质可以做燃料和造酒原料,也可以用来杀菌消毒
C. 物质C的结构简式为CH3CHO,E的名称为乙酸乙酯
D. B+D→E的化学方程式为:CH3CH2OH+CH3COOH→CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(化学式:POCl3)无色透明的带刺激性臭味的液体,熔点1.25℃、沸点1.5℃,在潮湿空气中剧烈发烟,易与水反应。常用作半导体掺杂剂及光导纤维原料。工业上,“氯化水解法”生产三氯氧磷的方法一般是将三氯化磷加入反应釜中,通入氯气,同时滴加水,控制氯水比在3.94左右,并控制氯气和水的通入速率,其流程如下:
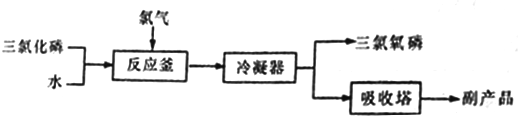
(1)在反应釜中将原料加热至105~109℃,“氯化水解法”生产三氯氧磷的化学方程式为___________。
(2)冷凝得到的粗三氯氧磷—般含有PCl3、H3PO3、PCl5和_________(填化学式)等杂质,进一步精制的方法是____________。
(3)已知H3PO3是—种易溶于水的二元弱酸。
①若将20 mL溶液与60 mL NaOH溶液等浓度混合并充分反应,化学方程式为______________。
②往废水中加入适量漂白粉并调节pH呈酸性,可将磷元素转化为磷酸钙沉淀回收,写出将H3PO3转化为磷酸钙的离子方程式:_____________________。
③经上述方法处理后的废水中c(PO43-) = 4×l0-7mol·L-1,溶液中c(Ca2+) =________mol·L-1。
(已知 Ksp[Ca3(PO4)2] = 2×10-29)
(4)工业上,还可以以三氯化磷为原料通过“氧气直接氧化法”制备三氯氧磷。从原理上看,与“氯化水解法”相比,该方法的优点是_______________________。(写出两点)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列微粒半径之比大于1的是 ( )
A. r (P) / r (Si) B. r (Be) / r (Mg) C. r(K) / r(Na) D. r(Cl) / r(Cl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0mol·L-1 的NaOH溶液 240mL
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移⑥洗涤 ⑦定容 ⑧冷却
本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、还有_________.
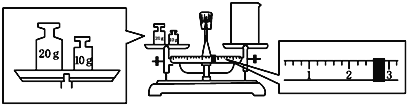
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图.烧杯的实际质量为__________g,要完成本实验该同学应称出__________gNaOH.
(3)使用容量瓶前必须进行的一步操作是_________________________________.
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是________________.
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与科技、社会、生产、生活等关系密切,下列有关说法不正确的是( )
A.苯酚不小心沾到皮肤上,可用酒精进行洗涤以减轻伤害
B.营养物质淀粉、纤维素和蛋白质都属于高分子化合物
C.提倡人们购物时不用塑料袋,是为了防止白色污染
D.35%-40%甲醛溶液俗称为福尔马林,可用来浸泡海产品来起到保鲜效果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是
A. Si的熔点高,可用作半导体材料 B. Cl2具有强氧化性,可用于漂白有色有机物质
C. Na2CO3溶液呈碱性,可用于洗涤油污 D. Al2O3硬度很大,可用于制造耐火材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列有机物:①正丁烷,②异丁烷,③正戊烷,④异戊烷,⑤新戊烷。物质沸点的排列顺序正确的是( )
A.①>②>③>④>⑤B.⑤>④>③>②>①C.③>④>⑤>①>②D.②>①>⑤>④>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com