
Ԫ��X��Y��Z��W��Ϊ������Ԫ�أ���ԭ����������������֪Yԭ������������
ռ�������������3/4��W����Z+��X+�뾶��С��������XW������Ϊ���壬Z�DZ���
���г�ϡ������Ԫ���⣬ԭ�Ӱ뾶����Ԫ�أ��ݴ˻ش��������⣺
��1��Z��Ԫ�����ڱ��е�λ�� ����ҵ������Z���ʵĻ�ѧ����ʽΪ
��2��A��B��Ϊ����������Ԫ���е�������ɵ�ǿ����ʣ��ҳ������������ʵ�ˮ��ҺpH
������7�����Ԫ�ص�ԭ����Ŀ�Ⱦ�Ϊ1��1��1����A������ˮ�ĵ��룬��B�ܴٽ�ˮ�ĵ�
�룬��A��B�Ļ�ѧʽ�ֱ�Ϊ �� ��
��3��C������������Ԫ�ص�������ɵ���Է�������Ϊ34�Ļ������C�ĵ���ʽ ��
��4����B�ڼ��������¿��Դ���CN���Ĺ�ҵ��ˮ���뽫����6������CN����CO32��
N2��OH����B�������ӣ�W�������ӣ��ֱ��������¶�Ӧ�ĺ����ϣ����һ����ƽ�����ӷ���ʽ�� + + �T + + + H2O
 ������ȫ�̼����ĩ���100��ϵ�д�
������ȫ�̼����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������a mol Na2SO3����Һ������b mol Na2S����Һ��Ϻ��������������ټ���ϡ���ᣬ����������dz��ɫ��������й���������ȷ����(����)
A����a��b��1��2������S��SO2
B����a��b��1��2����S����SO2
C����a��b��1��2������S��H2S
D����a��b��1��3������S��SO2��H2S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���ݻ����ܱ������з�����Ӧ��X(g)��Y(g)  Z(g)��W(s)����H>0������ʼͶ��1 mol X��1 mol Y����һ�������´ﵽƽ�⣬�ı���������仯��ϵ���ϼס���ͼ�������й��ж���ȷ����
Z(g)��W(s)����H>0������ʼͶ��1 mol X��1 mol Y����һ�������´ﵽƽ�⣬�ı���������仯��ϵ���ϼס���ͼ�������й��ж���ȷ����
A����ͼ��ʾ�¶ȶ�Xת���ʵ�Ӱ�죬�Ң��¶Ƚϵ�
B����ͼһ����ʾѹǿ��X���������Ӱ�죬�Ң�ѹǿ�ϸ�
C����ͼһ����ʾѹǿ��X���������Ӱ�죬�Ң�ѹǿ�ϸ�
D���ס���ͼ�����Ա�ʾ�¶ȡ�ѹǿ��ƽ���Ӱ�죬�Ң�>��<��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���г�ȥ���ʵķ�����ȷ����
A����ȥN2�е�����O2��ͨ�����ȵ�CuO��ĩ���ռ�����
B����ȥCO2�е�����HCl��ͨ��Na2CO3��Һ���ռ�����
C����ȥFeCl2��Һ�е�����FeCl3������������м����ַ�Ӧ����
D����ȥKCl��Һ�е�����MgCl2����������NaOH��Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪����ԭ��HSO3¯>I¯��������IO3¯> I2 ���ں�3 mol NaHSO3����Һ����μ���KIO3
 ��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��������ͼ
��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��������ͼ
��ʾ������˵������ȷ����
A��0~b�䷴Ӧ��3HSO3��+ IO3���� 3SO4����+ I��+ 3H��
B��a��ʱ����NaHSO3�����ʵ���Ϊ1.2 mol
C��b~c�䷴Ӧ��I2������������
D������Һ��I¯��I2�����ʵ���֮��Ϊ5��2ʱ�������
KIO3 Ϊ1.08mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����и�������ԭ��Ӧ�У�ˮ�Ȳ�����������Ҳ������ԭ������ ( )
A. 2F2+2H2O==4HF+O2 B. C+H2O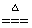 CO+H2
CO+H2
C. 2Na+2H2O==2NaOH+H2�� D. Cl2+H2O==HCl+HClO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������з�Ӧ�ж��й����ʻ�ԭ����ǿ������˳���� ( )
H2SO3+I2+H2O==2HI+H2SO4 2FeCl3+2HI==2FeCl2+2HCl+I2
3FeCl2+4HNO3==2FeCl3+NO��+2H2O+Fe(NO3)3
A. H2SO3>I->Fe2+>NO B. I->Fe2+>H2SO3>NO
C. Fe2+>I->H2SO3>NO D. NO>Fe2+>H2SO3>I-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
R��X��Y��Z������Ԫ�أ��䳣�����ϼ۾�Ϊ+2�ۣ���X2+�뵥��R����Ӧ��X2++Z=X+Z2+��Y+Z2+=Y2++Z�����������ӱ���ԭ��0�۽����ֵ������Դ�С����
A��R2+>X2+>Z2+>Y2+ B��X2+>R2+>Y2+>Z2+ C��Y2+>Z2+>R2+>X2+ D��Z2+>X2+>R2+>Y2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z��W���ֶ�����Ԫ����Ԫ�����ڱ��е����λ����ͼ��ʾ��������Ԫ��ԭ�ӵ�����������֮��Ϊ20�������ж���ȷ����
| W | X | Y |
| Z |
�� A�� ����Ԫ�ص�ԭ�Ӱ뾶��rZ��rX��rY��rW
�� B�� ����Ԫ���γɵĵ��������6��
�� C�� ����Ԫ�ؾ�������Ԫ���γɵ�������Ϊ18�ķ���
�� D�� ����Ԫ���У�Z������������Ӧ��ˮ����������ǿ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com