
下列各种情况下一定能大量共存的离子组为( )
A.pH=7的溶液中:Fe3+、Cl-、Na+、NO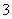
B.由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、CO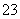 、Cl-、K+
、Cl-、K+
C.pH=1的溶液中:NH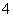 、Cl-、Cu2+、SO
、Cl-、Cu2+、SO
D.无色溶液中:Al3+、HCO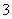 、I-、K+
、I-、K+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
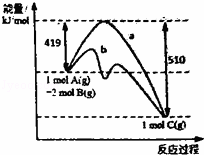
反应A(g)+2B(g)=C(g)的反应过程中能量变化如图所示.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.下列相关说法正确的是( )
|
| A. | 该反应是吸热反应 |
|
| B. | 催化剂改变了该反应的焓变 |
|
| C. | 催化剂降低了该反应的活化能 |
|
| D. | 该反应的焓变△H=﹣510kJ.mo1﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应 H2(g)+I2(g)⇌2HI(g)的平衡常数K1;反应HI(g)⇌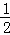 H2(g)+
H2(g)+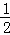 I2(g)的平衡常数K2,则K1、K2的关系为(平衡常数为同温度下的测定值)( )
I2(g)的平衡常数K2,则K1、K2的关系为(平衡常数为同温度下的测定值)( )
|
| A. | K1=2K2 | B. | K1=K22 | C. | K1= | D. | K1= |
查看答案和解析>>
科目:高中化学 来源: 题型:
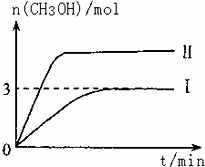
T10C 时,将9molCO2和12molH2充入3L密闭容器中,发生反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H<0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P.改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示.下列说法正确的是
( )
|
| A. | 曲线II对应的条件改变是减小压强 |
|
| B. | 若T2°C时上述反应的平衡常数为0.42,则T2<T1 |
|
| C. | 在T10C,若起始时向容器中充入5 mol CO2、5 mol H2、5 mol CH3OH(g)和 5 mol H2O(g),则达平衡前v(正)>v(逆) |
|
| D. | 在T10C,若起始时向容器中通入4.5molCO2、6mol H2,平衡时容器内的压强P1=P/2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.二氧化硫溶于水能导电,故二氧化硫属于电解质
B.硫酸钡难溶于水,故硫酸钡属于弱电解质
C.硫酸是强电解质,故纯硫酸能导电
D.氢氧根离子浓度相同的氢氧化钠溶液和氨水导电能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列浓度关系正确的是( )
A.氯水中:c(Cl2)=2
B.氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.等体积等浓度的氢氧化钠溶液与醋酸混合:c(Na+)=c(CH3COO-)
D.Na2CO3溶液中:c(Na+)>c(CO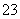 )>c(OH-)>c(HCO
)>c(OH-)>c(HCO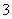 )>c(H+)
)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
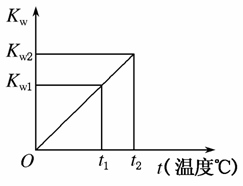
水的离子积常数Kw与温度t(℃)的关系如图所示:
(1)若t1=25 ℃,则Kw1=________;若t2=100 ℃时,Kw2=10-12,则此时0.05mol·L-1的Ba(OH)2溶液的pH=________。
(2)已知25 ℃时,0.1 L 0.1mol·L-1的NaA溶液的pH=10,则NaA溶液中所存在的平衡有:_______________________。
溶液中各离子的物质的量浓度由大到小的顺序为:________。
(3)25 ℃时,将pH=11的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=9,则NaOH溶液与硫酸溶液的体积比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
3.(1分)(2009•天心区校级模拟)下列关于糖的说法错误的是( )
|
| A. | 淀粉是一种天然高分子化合物 |
|
| B. | 糖都能水解 |
|
| C. | 纤维素没有甜味 |
|
| D. | 糖类是人体内能量的主要来源之一 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com