
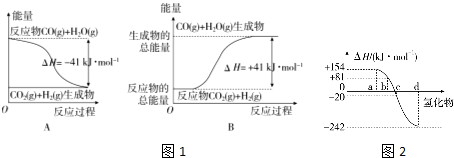
·ÖĪö £Ø1£©¢ŁĶ¼Ļó·ÖĪö·“Ó¦ĪļÄÜĮæøßÓŚÉś³ÉĪļæÉÖŖĪŖ·ÅČČ·“Ó¦£¬±ź×¢ĪļÖŹ¾Ū¼ÆדĢ¬ŗĶ¶ŌÓ¦·“Ó¦µÄģŹ±äŠ“³öČČ»Æѧ·½³ĢŹ½£»
¢ŚĶ¼Ļó·ÖĪöÉś³ÉĪļÄÜĮæøßÓŚ·“Ó¦ĪļæÉÖŖĪŖĪüČČ·“Ó¦£¬Ōņøł¾ŻĶ¼ĻóøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO2£Øg£©+H2£Øg£©ØTCO£Øg£©+H2O£Øg£©”÷H=+41kJ/mol£¬ÓÖĘųĢ¬Ė®±ä³ÉŅŗĢ¬Ė®»¹ŅŖ·ÅČČ£¬¾Ż“ĖÅŠ¶Ļ£»
£Ø2£©øł¾ŻČČ»Æѧ·½³ĢŹ½µÄŹéŠ“·½·ØæÉÖŖ£¬»Æѧ¼ĘĮæŹżÓė·“Ó¦ČČ³ÉÕż±Č£¬²¢×¢Ņā±źĆ÷ĪļÖŹµÄ¾Ū¼ÆדĢ¬Ą“½ā“š£»
£Ø3£©¢Łøł¾ŻŌŖĖŲÖÜĘŚĀÉ£¬Ķ¬Ņ»Ö÷×åŌŖĖŲ·Ē½šŹōŠŌŌ½Ēæ£¬Éś³ÉĘųĢ¬Ēā»ÆĪļŌ½ČŻŅ×£¬ĘųĢ¬Ēā»ÆĪļŌ½ĪČ¶Ø£»¶ųøł¾ŻČČĮ¦Ń§£¬ÄÜĮæŌ½µĶŌ½ĪČ¶Ø£¬ŅŌ“Ė½ųŠŠÅŠ¶Ļ£»
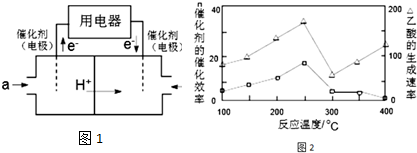
¢Śøł¾ŻĶ¼ĻóÅŠ¶Ļ³öabcd¶ŌÓ¦µÄø÷Ēā»ÆĪļ£¬øł¾ŻģŹ±äµÄ“󊔏銓ČČ»Æѧ·½³ĢŹ½£®
½ā“š ½ā£ŗ£Ø1£©Ķ¼Ļó·ÖĪöæÉÖŖĪŖ·ÅČČ·“Ó¦£¬·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO£Øg£©+H2O£Øg£©=CO2£Øg£©+H2£Øg£©”÷H=-41 kJ/mol£¬
¹Ź“š°øĪŖ£ŗCO£Øg£©+H2O£Øg£©=CO2£Øg£©+H2£Øg£©”÷H=-41 kJ/mol£»
¢ŚĶ¼Ļó·ÖĪöÉś³ÉĪļÄÜĮæøßÓŚ·“Ó¦ĪļæÉÖŖĪŖĪüČČ·“Ó¦£¬Ōņøł¾ŻĶ¼ĻóøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO2£Øg£©+H2£Øg£©ØTCO£Øg£©+H2O£Øg£©”÷H=+41kJ/mol£¬
A£®½«·“Ó¦µÄ·“Ó¦ĪļÓėÉś³ÉĪļÅŖ·“ĮĖ£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO2£Øg£©+H2£Øg£©ØTCO£Øg£©+H2O£Øg£©”÷H=+41kJ/mol£¬¹ŹA“ķĪó£»
B£®Éś³ÉĪļµÄÄÜĮæ±Č·“Ó¦ĪļµÄÄÜĮæøߣ¬¹ŹøĆ·“Ó¦ĪŖĪüČČ·“Ó¦£¬¹ŹBÕżČ·£»
C£®Éś³ÉĪļµÄÄÜĮæ±Č·“Ó¦ĪļµÄÄÜĮæøߣ¬¹ŹøĆ·“Ó¦ĪŖĪüČČ·“Ó¦£¬¹ŹC“ķĪó£»
D£®ŅņĪŖĘųĢ¬Ė®±ä³ÉŅŗĢ¬Ė®»¹ŅŖ·ÅČČ£¬µ±H2OĪŖŅŗĢ¬Ź±£¬Ęä·“Ó¦ČČÖµ“óÓŚ41kJ/mol£¬Ōņ”÷H£¼+41kJ•mol-1£¬¹ŹD“ķĪó£»
¹Ź“š°øĪŖ£ŗB£»
£Ø2£©16g¹ĢĢåĮņĶźČ«Č¼ÉÕŹ±·Å³ö148.4kJµÄČČĮ棬Ōņ1molSĶźČ«Č¼ÉÕŹ±·Å³ö·Å³ö296.8kJČČĮ棬ŌņČČ»Æѧ·½³ĢŹ½ĪŖ£ŗS£Øs£©+O2£Øg£©=SO2£Øg£©”÷H=-296.8 kJ/mol£¬
¹Ź“š°øĪŖ£ŗS£Øs£©+O2£Øg£©=SO2£Øg£©”÷H=-296.8 kJ/mol£»
£Ø3£©¢Ł·Ē½šŹōŌŖĖŲĒā»ÆĪļµÄĪČ¶ØŠŌÓėÉś³É1molĒā»ÆĪļŹ±µÄ”÷HµÄ¹ŲĻµĪŖ£ŗøł¾ŻŌŖĖŲÖÜĘŚĀÉ£¬Ķ¬Ņ»Ö÷×åŌŖĖŲ·Ē½šŹōŠŌŌ½Ēæ£¬Éś³ÉĘųĢ¬Ēā»ÆĪļŌ½ČŻŅ×£¬ĘųĢ¬Ēā»ÆĪļŌ½ĪČ¶Ø£¬¶ųÄÜĮæŌ½µĶŌ½ĪČ¶Ø£¬ĖłŅŌa”¢b”¢c”¢dŅĄ“ĪĪŖ£ŗH2Te”¢H2Se”¢H2S”¢H2O£¬
¹Ź“š°øĪŖ£ŗ·Ē½šŹōŌŖĖŲĒā»ÆĪļŌ½ĪČ¶Ø£¬”÷HŌ½Š”£¬·“Ö®ŅąČ»£»
¢ŚÓÉ¢ŁæÉÖŖ£¬bĪŖĪų»ÆĒāµÄÉś³ÉČČŹż¾Ż£¬ŌņĪų»ÆĒā·Ö½āĪüČČ£¬”÷H=-81kJ/mol£¬ĖłŅŌH2Se·¢Éś·Ö½ā·“Ó¦µÄČČ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗH2Se£Øg£©=Se£Øs£©+H2£Øg£©”÷H=-81kJ/mol£¬
¹Ź“š°øĪŖ£ŗH2Se£Øg£©=Se£Øs£©+H2£Øg£©”÷H=-81kJ/mol£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦µÄÄÜĮæ±ä»Æ£¬Ķ¼Ļó·ÖĪöÅŠ¶ĻŅŌ¼°øĒĖ¹¶ØĀɵÄÓ¦ÓĆ£¬×¢Ņā·“Ó¦ČČ”÷H=·“Ó¦ĪļÄÜĮæ×ÜŗĶ-Éś³ÉĪļÄÜĮæ×ÜŗĶ£¬ĢāÄæÄѶČÖŠµČ£¬²ąÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÄŃČܵē½āÖŹµÄČܶȻżŌ½Š”£¬Čܽā¶ČŌ½“ó | |
| B£® | æÉŅŌĶعż³Įµķ·“Ó¦Ź¹ŌÓÖŹĄė×ÓĶźČ«³Įµķ | |
| C£® | ÄŃČܵē½āÖŹµÄČܽāĘ½ŗāŹĒŅ»ÖÖ¶ÆĢ¬Ę½ŗā | |
| D£® | AgCl¹ĢĢåŌŚµČÅØ¶ČµÄNaCl”¢CaCl2ČÜŅŗÖŠµÄČܽā¶ČĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
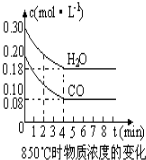 ŌŚŅ»Ģå»żĪŖ10LµÄČŻĘ÷ÖŠ£¬ĶØČėŅ»¶ØĮæµÄCOŗĶH2O£¬ŌŚ850”ꏱ·¢ÉśČēĻĀ·“Ó¦£ŗCO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2 £Øg£©”÷H£¼0£¬COŗĶH2OÅØ¶Č±ä»ÆČēĶ¼£®
ŌŚŅ»Ģå»żĪŖ10LµÄČŻĘ÷ÖŠ£¬ĶØČėŅ»¶ØĮæµÄCOŗĶH2O£¬ŌŚ850”ꏱ·¢ÉśČēĻĀ·“Ó¦£ŗCO£Øg£©+H2O£Øg£©?CO2£Øg£©+H2 £Øg£©”÷H£¼0£¬COŗĶH2OÅØ¶Č±ä»ÆČēĶ¼£®| Ź±¼ä£Ømin£© | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Įņ»ÆŠæ×Ŗ»Æ³ÉĶĄ¶µÄĄė×Ó·½³ĢŹ½ĪŖZnS£Øs£©+Cu2+£Øaq£©=Zn2+£Øaq£©+CuS£Øs£© | |
| B£® | ŌŚ°×É«Įņ»ÆŠæ×ĒŅŗÖŠµĪ¼ÓĻõĖįĒ¦ČÜŅŗ£¬²»»įÉś³ÉŗŚÉ«³Įµķ£ØPbS£© | |
| C£® | ŌŚĖ®ÖŠµÄČܽā¶Č£ŗS£ØZnS£©£¾S£ØPbS£©£¾S£ØCuS£© | |
| D£® | ČōČÜŅŗÖŠc£ØCu2+£©=1”Į10-10mol•L-1£¬ŌņS2-ŅŃĶźČ«×Ŗ»Æ³ÉCuS |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5.0 mol/L | B£® | 0.50 mol/L | C£® | 1.0 mol/L | D£® | 0.10 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µē½āAlCl3±„ŗĶČÜŅŗ£¬æÉÖĘµĆ½šŹōĀĮ | |
| B£® | ĀĮČČ·“Ó¦²»½ö±»ÓĆÓŚŗø½ÓøÖ¹ģ£¬¶ųĒŅ»¹³£±»ÓĆÓŚŅ±Į¶ČŪµć½ĻøߵĽšŹō | |
| C£® | ĀĮ±ČĢś»īĘĆ£¬µ«ĀĮÖĘĘ·±ČĢśÖĘĘ·ŌŚæÕĘųÖŠÄĶøÆŹ“ | |
| D£® | Al2O3”¢MgOµÄČŪµćŗÜøߣ¬æÉÓĆÓŚÖĘ×÷ÄĶøßĪĀ²ÄĮĻ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com