
| A. | FeCl2溶液【FeCl3】:加足量铁粉 | B. | NaCl溶液【Na2SO4】:用Ba(OH)2溶液 | ||
| C. | Na2CO3固体【NaHCO3】:加热 | D. | 铁粉【铝粉】:用NaOH溶液 |
分析 A、FeCl3能和Fe反应;
B、Na2SO4和Ba(OH)2反应生成硫酸钡和氢氧化钠;
C、NaHCO3受热分解;
D、铝粉和氢氧化钠溶液反应,而铁和氢氧化钠不反应.
解答 解:A、FeCl3能和Fe反应生成FeCl2,故能除去FeCl3,故A正确;
B、Na2SO4和Ba(OH)2反应生成BaSO4和NaOH,由引入了NaOH杂质,故B错误;
C、NaHCO3受热分解:2NaHCO3$\frac{\underline{\;△\;}}{\;}$Na2CO3+CO2↑+H2O,故可以用加热的方法除去NaHCO3,故C正确;
D、铝粉和氢氧化钠溶液反应,而铁和氢氧化钠不反应,故可以用氢氧化钠溶液除去铝,故D正确.
故选B.
点评 本题考查物质的除杂,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握物质的性质,难度不大.


科目:高中化学 来源: 题型:解答题
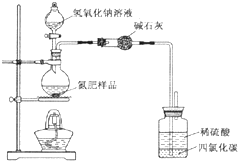 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:| 氢氧化钠溶液体积/mL | 40.00mL | ||
样品质量/g | 7.750 | 15.50 | 23.25 |
氨气质量/g | 1.870 | 1.870 | 1.700 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 砂滤是利用过滤原理除去水中较大的固体颗粒 | |
| B. | 臭氧可以消毒杀菌是因为臭氧有强氧化性 | |
| C. | 游泳池水中的臭氧浓度越大越好 | |
| D. | 活性炭可以吸附水中悬浮的杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②③④ | C. | ①②③⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
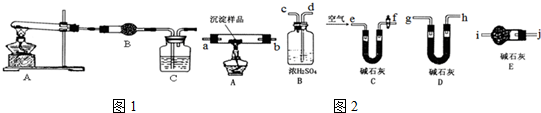
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
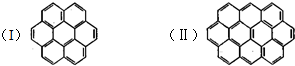 有两个或两个以上的苯环以共有环边的方式相互稠合的多环芳香烃称为稠环芳香烃.下图中椭圆烯也属于稠环芳香烃.据此回答:
有两个或两个以上的苯环以共有环边的方式相互稠合的多环芳香烃称为稠环芳香烃.下图中椭圆烯也属于稠环芳香烃.据此回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L CCl4含有4nA个Cl原子 | |
| B. | 7.8 g Na2O2与足量水反应转移0.2nA个电子 | |
| C. | 0.1 mol•L-1NaCl溶液中含有0.1nA个Na+ | |
| D. | 常温常压下,23 gNO2、N2O4混合气体中含有nA个氧原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com