
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 葡萄糖和果糖的分子式均为C6H12O6,二者互为同系物 | |
| D. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
分析 A.苯与溴水不反应;
B.甲烷和Cl2的反应为取代反应,乙烯中含双键;
C.分子式均为C6H12O6,结构不同;
D.乙酸与乙醇的酯化反应为取代反应,乙酸乙酯的水解反应为取代反应,且乙酸与碳酸钠反应后与乙酸乙酯分层.
解答 解:A.苯与溴水不反应,发生萃取,而乙烯与溴水发生加成反应使其褪色,原理不同,故A错误;
B.甲烷和Cl2的反应为取代反应,乙烯中含双键,则乙烯与Br2的反应为加成反应,反应不同,故B错误;
C.分子式均为C6H12O6,结构不同,二者互为同分异构体,故C错误;
D.乙酸与乙醇的酯化反应为取代反应,乙酸乙酯的水解反应为取代反应,且乙酸与碳酸钠反应后与乙酸乙酯分层,然后分液可除去乙酸乙酯中的少量乙酸,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应、同分异构体等为解答的关键,综合性较强,注重基础知识的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
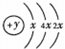 ,B、C可形成离子化合物B3C2,E是同周期元素中原子半径最小的元素.
,B、C可形成离子化合物B3C2,E是同周期元素中原子半径最小的元素. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A为周期表中原子半径最小的元素,B、C、D均为第二周期元素,其中B、C、D的电负性:D>C>B,第一电离能:C>D>B,且C无空轨道;E与A同主族,与F、G同周期,F为短周期金属元素,其单质既可以与酸又可以与碱反应放出H2.G的电子最外层中没有空轨道,且成对电子所占有的轨道数是未成对电子所占轨道数的3倍.
已知A为周期表中原子半径最小的元素,B、C、D均为第二周期元素,其中B、C、D的电负性:D>C>B,第一电离能:C>D>B,且C无空轨道;E与A同主族,与F、G同周期,F为短周期金属元素,其单质既可以与酸又可以与碱反应放出H2.G的电子最外层中没有空轨道,且成对电子所占有的轨道数是未成对电子所占轨道数的3倍.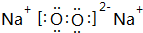 .它与F2D3按物质的量之比为1:1混合后投入水中,所发生反应的化学方程式为2Na2O2+2Al2O3=4NaAlO2+O2↑.
.它与F2D3按物质的量之比为1:1混合后投入水中,所发生反应的化学方程式为2Na2O2+2Al2O3=4NaAlO2+O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 银氨溶液可用于检验淀粉是否发生水解 | |
| B. | 植物油的主要成分是高级脂肪酸 | |
| C. | 蔗糖及其水解产物均可发生银镜反应 | |
| D. | 鸡蛋清溶液中加入饱和硫酸钠溶液,生成的沉淀物不能再溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将一定量的氯气通入30 mL浓度为10.0mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系,n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 | |
| B. | 实验室可以配制一种仅含Al3+、K+、SO42-、NO3-这4种离子(不考虑来源于水电离的离子)的溶液,且4种离子的浓度均为1mol/L | |
| C. | HCl、FeCl3、Fe3O4、NaOH都可通过置换反应一步得到也可通过化合反应一步得到 | |
| D. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol C6H14分子中共价键总数为20NA | |
| B. | 1mol乙基(-CH2CH3)电子总数17NA | |
| C. | 常温常压下,26g苯乙烯和苯组成的混合物中所含有的碳原子数为4NA | |
| D. | 标准状况下,22.4L甲醇的分子数中所含羟基数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇汽油推广的最主要的目的在于降低国际市场的油料价格 | |
| B. | 生物柴油燃烧不会产生二氧化碳,是一种清洁能源 | |
| C. | 太阳能是一种清洁安全的不可再生能源 | |
| D. | 纳米金属燃料表面积大,易引发,能量释放快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
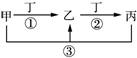 甲、乙、丙、丁是中学常见的物质,其中甲、乙、丙均含有同一种元素,在一定条件下的转化关系见图,下列说法正确的是( )
甲、乙、丙、丁是中学常见的物质,其中甲、乙、丙均含有同一种元素,在一定条件下的转化关系见图,下列说法正确的是( )| A. | 若丁为用量最大,用途最广的金属单质,乙的溶液一定为FeCl3 | |
| B. | 若通常情况下甲、乙、丙、丁都是气体,且乙和丁为空气的主要成分,则反应①的化学方程式为4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O | |
| C. | 若甲、乙、丙的溶液显碱性,则丙可能可以作为医疗上治疗胃酸过多症的药剂 | |
| D. | 若丁为化合物,且为氯碱工业的重要产品,则甲一定为含Al3+的盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R | B. | 单质与稀盐酸反应的快慢为L<Q | ||
| C. | M与T形成的化合物是离子化合物 | D. | L2+与R2-的核外电子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com