
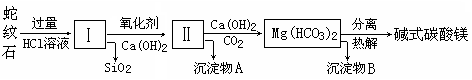
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
 Fe(OH)3+3H+和Al3++3H2O
Fe(OH)3+3H+和Al3++3H2O Al(OH)3+3H+,只要加入一种能消耗H+的物质即可使上述水解平衡向正反应方向移动,除去Fe3+、Al3+,该方案使用加Ca(OH)2的方法,但此步加入Ca(OH)2不能太多,需将溶液的pH控制在7~8。若pH小于7,Al3+不能完全沉淀;若pH过高导致生成的Al(OH)3又发生反应Al(OH)3+OH-=AlO2-+2H2O而溶解,同时Mg2+也转化为沉淀而损失。
Al(OH)3+3H+,只要加入一种能消耗H+的物质即可使上述水解平衡向正反应方向移动,除去Fe3+、Al3+,该方案使用加Ca(OH)2的方法,但此步加入Ca(OH)2不能太多,需将溶液的pH控制在7~8。若pH小于7,Al3+不能完全沉淀;若pH过高导致生成的Al(OH)3又发生反应Al(OH)3+OH-=AlO2-+2H2O而溶解,同时Mg2+也转化为沉淀而损失。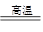 (a+b)MgO+aCO2↑+(b+c)H2O↑,需要测定的数据是①样品质量;②MgO质量;③生成CO2的质量(或体积);④生成水的质量。
(a+b)MgO+aCO2↑+(b+c)H2O↑,需要测定的数据是①样品质量;②MgO质量;③生成CO2的质量(或体积);④生成水的质量。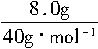 =0.2mol
=0.2mol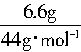 =0.15mol
=0.15mol  =0.2mol
=0.2mol

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
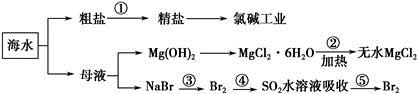
| A.整个过程可在实验室中模拟进行 |
| B.工段②是风化过程 |
| C.在工段③④⑤中溴元素均被氧化 |
D.工段①中除去粗盐中的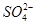 、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
| B.用过量氨水除去Fe3+溶液中的少量Al3+ |
| C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 |
| D.Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


| A.b曲线表示的是向X溶液中加入NaOH溶液 |
| B.在O点时两方案中所得溶液浓度相等 |
| C.a、b曲线表示的反应都是非氧化还原反应 |
| D.X溶液显酸性,Y溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
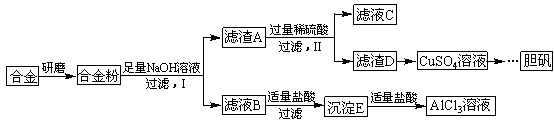
 2CuO,CuO+H2SO4=CuSO4+H2O
2CuO,CuO+H2SO4=CuSO4+H2O CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.此法的优点之一是原料来源丰富 |
| B.进行①、②、③步操作的目的是从海水中提取氯化镁 |
| C.第④步电解时会产生氯气 |
| D.以上提取镁的过程中涉及的反应有分解反应、化合反应、复分解反应和置换反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(1)(2)(3)(4) | B.(1)(2)(4)(3) | C.(2)(3)(4)(1) | D.(3)(1)(4)(2) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
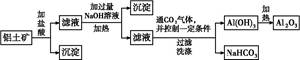
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com