
| A. | 金属活动性B>A | |
| B. | 还原性B>A | |
| C. | 在后者装置中金属A发生还原反应,金属B发生氧化反应 | |
| D. | 金属B的表面上明显有气泡产生,金属A表面无气泡 |
分析 金属A和金属B分别放入稀H2SO4中均有氢气生成,说明A、B在金属活动性顺序表中都位于H之前;若将金属A和金属B相连后投入稀H2SO4中发现A被腐蚀,B未被腐蚀,说明金属活动性A大于B,金属的金属性越强,其单质的还原性越强,据此分析解答.
解答 解:金属A和金属B分别放入稀H2SO4中均有氢气生成,说明A、B在金属活动性顺序表中都位于H之前;若将金属A和金属B相连后投入稀H2SO4中发现A被腐蚀,B未被腐蚀,说明金属活动性A大于B,
A.通过以上分析知,金属活动性A>B,故A错误;
B.金属的金属性越强其单质的还原性越强,金属性A>B,所以还原性A>B,故B错误;
C.在后者装置中金属A失电子发生氧化反应,金属B上得电子发生还原反应,故C错误;
D.A失电子发生氧化反应生成阳离子进入溶液,B电极上氢离子得电子生成氢气,所以B电极上有气泡生成,故D正确;
故选D.
点评 本题以原电池原理为载体考查金属活动性强弱判断,为高频考点,金属的金属性强弱与失电子难易程度有关,与失电子多少无关,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 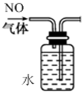 排水法收集NO | |
| B. | 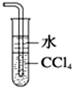 吸收尾气中少量NH3或HCl,并防止倒吸 | |
| C. |  制取并收集少量NH3 | |
| D. | 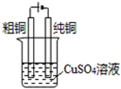 电解精炼铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Na、K | B. | Ba2+、Ca2+、Mg2+ | C. | K+、Ca2+、Cl- | D. | N、O、F |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2.4gMg和6.5g Zn | B. | Mg和Zn各2.5g | C. | Mg和Al各2.5g | D. | 2.3gNa和2.4gMg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广可利用太阳能、风能的城市照明系统 | |
| B. | 使用露天焚烧法处理未经分类的生活垃圾 | |
| C. | 加速建设地铁、轻轨等轨道交通,减少汽车尾气排放 | |
| D. | 积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
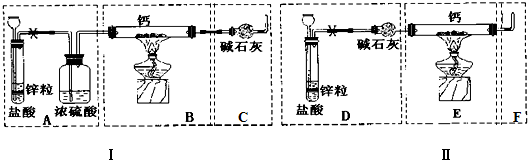
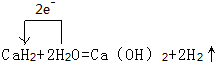 ,结合上述反应,实验结束后,甲同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此推断,上述实验确有CaH2生成.请你分析该同学的判断是否合理?(填“是”或“否”).若不合理解释原因(若判断合理,此问不用两答)否,金属钙和水反应也有相似的实验现象
,结合上述反应,实验结束后,甲同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此推断,上述实验确有CaH2生成.请你分析该同学的判断是否合理?(填“是”或“否”).若不合理解释原因(若判断合理,此问不用两答)否,金属钙和水反应也有相似的实验现象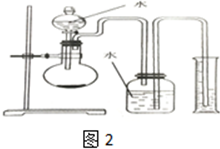
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
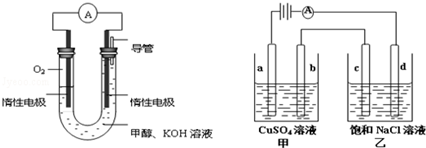
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7种和2种 | B. | 8种和3种 | C. | 42种和3种 | D. | 56种和3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
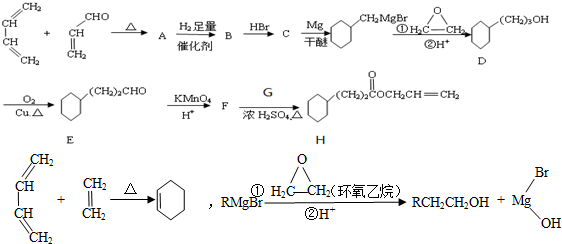
 ,G物质核磁共振氢谱共有4个峰.
,G物质核磁共振氢谱共有4个峰. .写出D生成E的化学方程式
.写出D生成E的化学方程式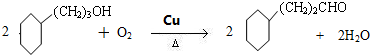 .
.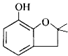 呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式:
呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式: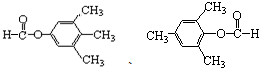 .
.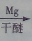 CH3CH2MgBr
CH3CH2MgBr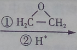 CH3CH2CH2CH2OH.
CH3CH2CH2CH2OH.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com