
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B.工业上冶炼活泼金属往往用电解的方法,如电解NaCl水溶液制备钠,电解Al2O3制Al |
| C.往往将闸门与直流电源的负极相连,这是牺牲阳极的阴极保护法 |
D.电解过程中,溶液中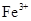 、 、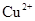 、 、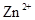 的氧化性依次减弱 的氧化性依次减弱 |
科目:高中化学 来源:不详 题型:单选题

| A.Zn为负极,Cu为正极 |
B.正极反应为 Zn - 2e- ="="  |
C.负极反应为Cu - 2e-="="  |
| D.该装置能将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


| A.反应开始时,乙中石墨电极上发生的电极反应式为2I——2e—===I2 |
| B.反应开始时,甲中石墨电极上Fe3+被还原 |
| C.电流计读数为零时,反应达到化学平衡状态 |
| D.电流计读数为零后,在甲中加入FeCl2固体,乙中石墨电极为负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜锌原电池中铜是正极 |
| B.用电解法精炼粗铜时用纯铜作阳极 |
| C.在镀件上电镀铜时镀件不作阴极 |
| D.电解稀硫酸制H2、O2时铜与电源正极相连 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.Zn、Zn | B.Zn、Cu | C.Cu、Cu | D.石墨、石墨 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com