
【题目】元素周期表中,位于金属元素与非金属元素的分界线附近的一些元素可用于生产()
A. 合金B. 农药C. 半导体D. 催化剂
科目:高中化学 来源: 题型:
【题目】下列有关化学反应的叙述正确的是( )
A.AlCl3溶液和过量氨水生成Al(OH)3B.Mg在CO2中燃烧生成MgCO3
C.Fe(OH)3溶于氢碘酸生成FeI3D.SiO2与H2O反应生成H2SiO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫和铁的各种化合物在日常生活中有着广泛应用,请结合所学知识回答下列问题:
(1)已知1g H2S气体完全燃烧,生成液态水和二氧化硫气体,放出17.24kJ热量,请写出H2S气体燃烧热的热化学方式: .
(2)已知常温下在NaHSO3溶液中c(H2SO3 )<c(SO32﹣) 且H2SO3 的电离平衡常数为:K1=1.5×10﹣2 K2=1.1×10﹣7;氨水的电离平衡常数为K=1.8×10﹣2; (i)则等物质的量浓度的下列三种溶液:①NH3H2O ②KHSO3 ③KHCO3 溶液中水的电离程度由大到小排列顺序为
(ii)0.1molL﹣1的NaHSO3溶液中C(H+)C(OH﹣)(“>”、“<”或“=”):
(3)已知25℃时Ksp[Cu(OH)2]=2.2×10﹣20 , Ksp[Fe(OH)2]=8.0×10﹣16 , KspFe(OH)3]=4.0×10﹣38 , Ksp[Al(OH)3]=1.1×10﹣33(i)在25℃下,向浓度均为0.1mol/L的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成沉淀(填化学式).
(ii)向1.0mol Fe2(SO4)3和1.0mol FeSO4的1L酸性混合溶液通入NH3 , 至该溶液的PH为3时,所得溶液中c(Fe2+):c(Fe3+)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用硫铁矿(主要成分FeS2)生产硫酸和绿矾(FeSO47H2O)的工业流程示意图如图: 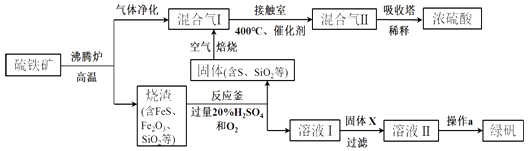
(1)沸腾炉中,硫铁矿进行粉碎处理的目的是 .
(2)接触室中,发生的主要反应是SO2与O2的反应,其化学方程式是 .
(3)反应釜中,烧渣经过反应转化为溶液I和固体. ①烧渣中的FeS在反应中做剂(填“氧化”或“还原”).
②溶液I中所含溶质的化学式是
(4)操作a的主要步骤是:加热浓缩、、过滤洗涤.
(5)流程中,固体X可以选择硫铁矿(FeS2)或;当固体X为硫铁矿(FeS2)时,将溶液I与固体X发生反应的离子方程式补充完整: FeS2++═Fe2++SO42﹣+ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,由水电离的c(H+)=1.0×l0-13mol/L的溶液中一定不可能大量存在的离子是
A. NH4+ B. HCO3- C. OH- D. Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列:①H2O ②H2O2③Ba(OH)2④Na2O2⑤Cl2⑥Ar⑦CO2等物质填空. (1﹣4小题填序号)
(1)由离子键和非极性键构成的是
(2)由极性键和非极性键构成的是
(3)不存在化学键的是
(4)共价化合物有
(5)写出下列物质的电子式:Na2O2 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)氧化铜矿用稀硫酸溶解后所得酸浸液(含Cu2+、H+、SO42﹣、Mg2+、A13+、Fe2+) 经下列流程可制得高纯度硫酸铜晶体如图1: 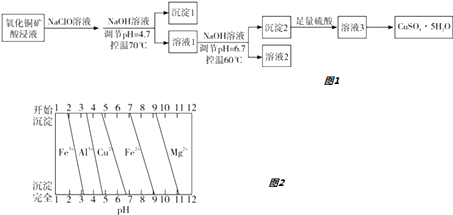
已知:该实验条件下,各金属离子沉淀的pH如图2所示.下列判断正确的是( )
A.沉淀1的主要成分为Al(OH)3和Fe(OH)3
B.溶液2中所含金属阳离子只有Mg2+
C.将溶液3蒸干即得CuSO45H2O晶体
D.若不加入NaClO溶液,对制得硫酸铜晶体的纯度将无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaNO2是一种食品添加剂,它与酸性KMnO4溶液发生反应 MnO4﹣+NO2﹣+X→Mn2++NO3﹣+H2O(未配平).下列叙述中正确的是( )
A.生成1 mol NaNO3需消耗0.4 mol KMnO4
B.反应过程中溶液的pH减小
C.该反应中NO ![]() 被还原
被还原
D.X可以是盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com