
【题目】已知A、B、C 均为短周期的元素,A、B同周期,A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构,下列说法中正确的是( )
A.离子半径:A2->C->B2+
B.C元素的最高正价一定为+7价
C.对应气态氢化物的稳定性:A>C
D.还原性:A2-<C-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①C3H6(g)+NH3(g)+![]() O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol
O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol
②C3H6(g)+ O2(g)=C3H4O(g)+H2O(g) ΔH=-353kJ/mol
两个反应在热力学上趋势均很大,其原因是________________;有利于提高丙烯腈平衡产率的反应条件是_____________;提高丙烯腈反应选择性的关键因素是___________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________________(填“是”或者“不是”)对应温度下的平衡
产率,判断理由是______________;高于460℃时,丙烯腈产率降低的可能原因是_____________(双选,填标号)
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应活化能增大
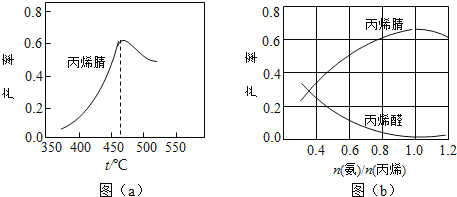
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为 ,理由是_________________。进料气氨、空气、丙烯的理论体积比约为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、工业上用粗氧化铜(含杂质FeO)为原料制取氯化铜晶体(CuCl2·2H2O)的生产过程中会产生沉淀氢氧化铁,用来制取FeCO3的流程如下:
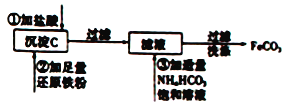
完成上述转化过程中的离子方程式
①____________________________。
②____________________________。
Ⅱ、有一瓶澄清溶液,其中可能含有可能含有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、NO3-、CO32-、SO42-。取该溶液进行以下实验:
(1)填写表中开空白:
实验步骤 | 肯定不存在的离子 |
①用PH试纸检验,溶液呈强酸性 | |
②取出部分溶液,加入少量CCl4和数滴新制氯水,振荡,精置CCl4层呈紫红色 | |
③另取出部分溶液,向其加入NaOH溶液,使溶液从酸性变为碱性,在滴加过程中及滴加完毕后,均无沉淀产生 | |
④取③中的部分碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝 | |
⑤另取③中的部分碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成 |
(2)根据以上事实,该溶液中肯定存在的离子是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数的值用NA表示,则:
(1)该气体的物质的量为 。
(2)该气体所含原子总数为________________个。
(3)该气体在标准状况下的体积为 L。
(4)该气体在标准状况下的密度为_______________ g/L。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为________________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(有机化学基础)胡椒乙酸是合成许多药用生物碱的重要中间体,以苯酚为原料制备胡椒乙酸的合成路线如图所示。
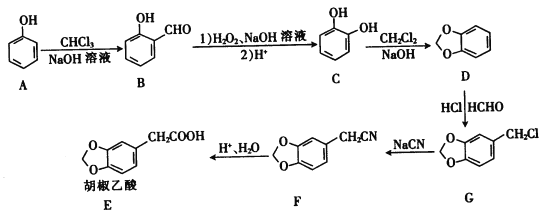
回答下列问题:
(1)下列关于有机物B的说法正确的是________(填字母)。
a.能与FeCl3溶液发生显色反应
b.核磁共振氢谱中只有3组峰
c.能发生银镜反应
d.能与溴水发生加成反应
(2)C的名称是__________,C→D的反应类型是__________。
(3)胡椒乙酸(E)中所含官能团的名称为______________。
(4)G生成F的化学方程式为____________。
(5)W是E的同分异构体,0.5molW与足量碳酸氢钠溶液反应生成1molCO2,已知W的苯环上只有2个取代基,则W的结构共有___________(不含立体异构)种,其中核磁共振氢谱有五组峰的结构简式为____________。
(6)参照上述合成路线,写出以一氯甲苯(![]() )为原料(无杌试剂任选)制备苯乙酸的合成路线:______________________。
)为原料(无杌试剂任选)制备苯乙酸的合成路线:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+3B(g)===4C(g)+2D(g),在相同时间内,用不同物质表示的平均反应速率如下,则反应速率最快的是( )
A.v(A)=0.4 mol/(L·s) B.v(B)=0.8 mol/(L·s)
C.v(C)=1.2 mol/(L·s) D.v(D)=0.7 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)及其化合物可用于制半导体及除草剂等。回答下列问题:
(1)砷是氮的同族元素,比氮多2个电子层,砷在周期表中的位置为第__________周期___________族;AsH3的热稳定性比NH3___________(填“强”或“弱”)。砷在自然界中丰度最大的核素的中子数为40,该核素为______________(用元素符号表示)。
(2)砷化镓是常见的半导体材料,Ga与As同周期,镓最外层有3个电子,砷化镓的化学式为____________。
(3)某工业废水中含有少量的As2O3,向该废水中通入硫化氢可将其转化为更难溶的As2S3,该反应的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O![]() HCl+HClO K=4.5×10-4。次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代。请回答:
HCl+HClO K=4.5×10-4。次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代。请回答:
(1)氯碱工业生产氯气的化学方程式为__________________________。
(2)84消毒液(主要成分为NaClO)与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为________________________。
(3)二氧化氯是一种高效、广谱、安全的杀菌、保鲜剂。我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为____________________。
(4)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧化性强弱的微型装置(如图)。

①下列溶液能吸收Cl2的是________(填字母序号)。
A.饱和食盐水
B.饱和Na2SO3溶液
C.饱和NaOH溶液
D.浓硫酸
②能说明Cl2的氧化性强于I2的实验现象是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com