
某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是

A.该反应的还原剂是Cl-
B.消耗1 mol还原剂,转移6 mol电子
C.氧化剂与还原剂的物质的量之比为2:3
D.反应后溶液的酸性明显增强
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年河北省高一上第一次月考化学卷(解析版) 题型:实验题
(Ⅰ)A、B、C三种无色可溶性盐分别是由Na+、Ag+、Ba2+、Cl—、NO3—、CO32—中不同的阴、阳离子所组成。经实验A溶液、B溶液均可与盐酸反应,其中A 产生白色沉淀,B产生气泡。则A为 、B为 、将B和C的溶液混合反应的化学方程式为: 。
(Ⅱ)一学生设计了如下实验方案分离NaCl和CaCl2两种固体的混合物。填空和回答下列问题:
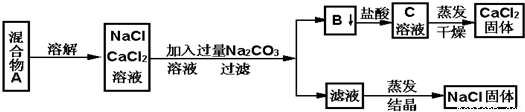
(1)B物质是 (写化学式)
(2)按此实验方案分离得到的NaCl,经分析含有杂质,此杂质的化学式为 ,因为上述方案中某一步设计有毛病,这一步的正确设计方案应是 。
(3)写出生成沉淀B的化学方程式 。
(4)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第三次月考化学卷(解析版) 题型:选择题
实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂。下列操作中可能使测定结果偏低的是
A.酸式滴定管在装酸液前未用标准盐酸润洗2~3次
B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.锥形瓶内溶液颜色的变化由黄色变为橙色时,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第三次月考化学卷(解析版) 题型:选择题
室温下pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
A.加适量的醋酸钠晶体后,两溶液的pH均增大
B.使温度都升高20℃后,两溶液的pH均不变
C.加水稀释2倍后,两溶液的pH均减小
D.加足量的锌充分反应后,两溶液中产生的氢气一样多
查看答案和解析>>
科目:高中化学 来源:2017届河北省石家庄市高三上第一次阶段考试化学卷(解析版) 题型:填空题
(1)氨气具有还原性,在铜的催化作用下, 氨气和氟气发生反应生成A和B。A为铵盐,B在标准状况下为气态。在此反应中,若有1体积氨气参加反应,则有0.75体积氟气参加反应;若有8.96 L氨气(标准状况)参加反应,则生成0.3 mol A。在标准状况下,生成2.24 L B,则该反应中转移电子的物质的量为 mol。
(2)将等物质的量Fe2O3与FeCl3置于密闭管中加热,能恰好完全反应,且只生成一种产物X,其物质的量是反应物总物质的量的1.5倍,写出X的化学式 ;
(3)完成以下氧化还原反应的离子方程式:
( )MnO4-+ SO32-+ = Mn2++ SO42-+
查看答案和解析>>
科目:高中化学 来源:2017届河北省石家庄市高三上第一次阶段考试化学卷(解析版) 题型:选择题
海带中提取碘的实验方法:①称取3 g干海带,用刷子把干海带表面的附着物刷净;②将海带剪碎,用酒精润湿(便于灼烧)后,放在坩埚中;③用酒精灯灼烧盛有海带的坩埚,至海带完全成灰,停止加热,冷却;④将海带灰转移到小烧杯中,再向烧杯中加入10 mL蒸馏水,搅拌,煮沸2~3 min,使可溶物溶解,过滤;⑤向滤液中滴入几滴硫酸,再加入约1 mL H2O2溶液,观察现象。下列说法正确的是
A.步骤①中也可以用水洗涤除去海带表面的附着物
B.步骤④过滤操作需要两种玻璃仪器
C .步骤⑤所得的溶液中加入淀粉可看到溶液变为蓝色
.步骤⑤所得的溶液中加入淀粉可看到溶液变为蓝色
D.通过以上①~⑤步骤即可得到纯度高的I2
查看答案和解析>>
科目:高中化学 来源:2017届河北省石家庄市高三上第一次阶段考试化学卷(解析版) 题型:选择题
利用下列实验装置能完成对应实验的是

A.量取20.00 mL Na2CO3溶液 B.能证明非金属性 Cl>C>Si
C.实验室制取并收集NH3 D.分离酒精与CCl4
查看答案和解析>>
科目:高中化学 来源:2017届安徽省等四校高三上10月联考化学试卷(解析版) 题型:选择题
水溶液X中只可能溶有Na+、Ca2+、Fe3+、AlO2-、SiO32-、SO32-、CO32-、SO42-中的若干种离子。某同学对该溶液迸行了如下实验:

下列判断正确的是
A.气体甲一定是纯净物
B.沉淀甲是硅酸和硅酸钙的混合物
C.Na+、AlO2-和SiO32-一定存在于溶液X中
D.CO32-和SO42-一定不存在于溶液X中
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第二次段考化学试卷(解析版) 题型:实验题
氰化钠是一种重要的基本化工原料,同时也是一 种剧毒物质,严重危害人类健康。一旦泄露需要及时处理,一般可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染。
种剧毒物质,严重危害人类健康。一旦泄露需要及时处理,一般可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻环境污染。
已知:氰化钠化学式为NaCN(C元素+2价,N元素-3价),氰化钠是一种白色结晶颗粒,剧毒,易溶于 水,水溶液呈碱性,易水解生成氰化氢。
水,水溶液呈碱性,易水解生成氰化氢。
(1)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是 。
(2)氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3═NaSCN+Na2SO3;已知:NaSCN中S为-2价,处理1molNaCN,反应中转移电子的物质的量为___________。
(3)CN—中C元素显+2价,N元素显—3价,则非金属性N__ _C(填“<”、“>”或“=”),请设计实验证明:_____________。
某化学兴趣小组实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】实验室通过下图装置制备Na2S2O3。

(4)b装置的作用是 。c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、N a2CO3,还可能有 。
a2CO3,还可能有 。
(5)实验结束后,在e处最好连接盛 (选填“NaOH溶液”、“水”、“CCl4”中任一种)的注射器,再关闭K2打开K1,防止拆除装置时污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水 中氰化钠的含量。
中氰化钠的含量。
已知:
①废水中氰化钠的最高排放标准为0.50mg/L。
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先与Ag+反应。
实验如下:
取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.000×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
(6)滴定终点的判断方法是 。
(7)处理后的废水是否达到排放标准 (填“是”或“否”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com