
【题目】炼铁厂的废渣铁矾渣主要含有K2Fe6(SO4)4(OH)12 、ZnO![]() Fe2O3 及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:
Fe2O3 及少量的CaO、MgO、SiO2 ,等等。可利用废渣铁矾渣制备复合镍锌铁氧体 (NiZnFe4O8.具体制备流程如下图所示:

(1)试剂1是过量的______。
(2)试剂2为过量的铁粉,加入后可以观察的现象有 ______________________。
(3)NH4F溶液不能放入玻璃器皿中保存,理由是_____________________________(用离子方程式表示)。已知:25 °C时,Ksp(CaF2)=2.7×10-11、,Ksp(MgF2)=6.4×10-19。加入NH4F溶液沉淀后,c(Mg2+) = 1. 6×10-10mol L-1,此时Ca2+是否也完全沉淀?写出具体的分析过程:______(若溶液中某离子浓度小于1.0×10-5mol L-1时,说明该离子已沉淀完全)。
(4)在Fe2+、Ni2+、Zn2+共沉淀过程中,若以Me代表Fe、Ni、Zn元素,则生成MeCO32Me(OH)2H2O沉淀的化学方程式为 ________________________________.
(5)按照上述流程,一座10万吨规模的炼铁厂每年产生铁矶渣约5万吨,Fe3+含量为44.8%,理论上每年至少可制备复合镍锌铁氧体(NiZnFe4O8 ,M=476 g mol -1 )__________万吨。
(6)滤液Ⅱ中加入的ZnSO4溶液,低温烘干后可得到皓矾(ZnSO4 7H2O) 取28.70 g皓矾加热至不同温度,剩余固体的质量变化如图所示:

①100 °C时所得固体的化学式__________ 。
②680 °C时所得固休的化学式为____
【答案】稀H2SO4(或稀硫酸) 溶液有棕黄色转变为浅绿色,同时有气泡产生 NH4+ +F-+H2O=NH3·H2O+HF、SiO2+ 4HF = SiF4 + 2H2O 已知25 °C时,Ksp(CaF2)=2.7×10-11、,Ksp(MgF2)=6.4×10-19。加入NH4F溶液沉淀后,c(Mg2+) = 1. 6×10-10mol L-1,则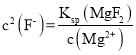 =4×10-9,故
=4×10-9,故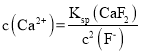 =0.675×10-2 mol L-1>1.0×10-5mol L-1,故Ca2+未完全沉淀; 3MeSO4+6NH4HCO3=MeCO32Me(OH)2H2O+5CO2↑ 7.6 ZnSO4 H2O Zn3O(SO4)2
=0.675×10-2 mol L-1>1.0×10-5mol L-1,故Ca2+未完全沉淀; 3MeSO4+6NH4HCO3=MeCO32Me(OH)2H2O+5CO2↑ 7.6 ZnSO4 H2O Zn3O(SO4)2
【解析】
(1)废渣铁矾渣主要含有K2Fe6(SO4)4(OH)12,在除杂制备过程中避免引入更多的离子,应该使用稀硫酸进行酸浸。
答案为:稀H2SO4(或稀硫酸)
(2)酸浸后的溶液含有三价铁离子的棕黄色溶液,加入过量铁粉,使三价铁离子转化为二价铁离子,溶液有棕黄色转变为浅绿色。酸浸时硫酸过量,加入铁粉有气泡产生。
答案为:溶液有棕黄色转变为浅绿色,同时有气泡产生。
(3)NH4F会水解生成氨水与HF,HF会腐蚀玻璃瓶,离子反应方程式为:NH4+ +F-+H2O=NH3·H2O+HF、SiO2+ 4HF = SiF4 + 2H2O;已知25 °C时,Ksp(CaF2)=2.7×10-11、,Ksp(MgF2)=6.4×10-19。加入NH4F溶液沉淀后,c(Mg2+) = 1. 6×10-10mol L-1,则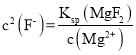 =4×10-9,故
=4×10-9,故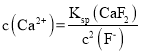 =0.675×10-2 mol L-1>1.0×10-5mol L-1,故Ca2+未完全沉淀;
=0.675×10-2 mol L-1>1.0×10-5mol L-1,故Ca2+未完全沉淀;
答案为:NH4+ +F-+H2O=NH3·H2O+HF、SiO2+ 4HF = SiF4 + 2H2O;已知25 °C时,Ksp(CaF2)=2.7×10-11、,Ksp(MgF2)=6.4×10-19。加入NH4F溶液沉淀后,c(Mg2+) = 1. 6×10-10mol L-1,则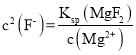 =4×10-9,故
=4×10-9,故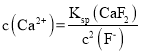 =0.675×10-2 mol L-1>1.0×10-5mol L-1,故Ca2+未完全沉淀;
=0.675×10-2 mol L-1>1.0×10-5mol L-1,故Ca2+未完全沉淀;
(4)根据流程Fe、Ni、Zn元素来的硫酸盐与NH4HCO3生成MeCO32Me(OH)2H2O沉淀和二氧化碳反应方程式为:3MeSO4+6NH4HCO3=MeCO32Me(OH)2H2O+5CO2↑;
故答案为: 3MeSO4+6NH4HCO3=MeCO32Me(OH)2H2O+5CO2↑;
(5)黄钾铁矾渣约5万吨,Fe3+含量为5万吨×48%=2.4万吨,根据2Fe3++Fe=3Fe2+,
则Fe2+含量为2.4万吨×![]() =3.6万吨,设制得的NiZnFe4O8有x万吨,根据元素守恒,有
=3.6万吨,设制得的NiZnFe4O8有x万吨,根据元素守恒,有![]() =3.6,解得x=7.6万吨。
=3.6,解得x=7.6万吨。
答案为:7.6
(6)皓矾(ZnSO4 7H2O)受热易分解,在不同的温度下分解可生成ZnSO4 H2O或ZnSO4或ZnO或Zn3O(SO4)2产物不同;28.70 g皓矾的物质的量为:
![]() , 不论分解产物是什么,根据锌元素守恒,物质的量为
, 不论分解产物是什么,根据锌元素守恒,物质的量为![]() ,因此生成
,因此生成![]() ZnSO4 H2O的质量为17.90g;生成
ZnSO4 H2O的质量为17.90g;生成![]() ZnSO4的质量为16.10g;生成
ZnSO4的质量为16.10g;生成![]() Zn3O(SO4)2的质量为13.34g;生成
Zn3O(SO4)2的质量为13.34g;生成![]() ZnO的质量为8.10g;
ZnO的质量为8.10g;
根据上述
① 100 °C时所得固体的为17.90g,生成的固体为ZnSO4 H2O。
② 680 °C时所得固休的质量为13.43g化学式为Zn3O(SO4)2。
答案为:ZnSO4 H2O;Zn3O(SO4)2


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 25 ℃时,向水中加入少量固体NaHSO4,c(H+)增大,Kw不变
B. 向0.1 mol·L-1CH3COOH溶液中加入少量的CH3COONa晶体,  减小
减小
C. 常温下,向BaCO3饱和溶液中加入Na2CO3固体,c(Ba2+)减小,BaCO3的Ksp减小
D. 一定条件下,将一定浓度的CH3COONa溶液加水稀释,溶液中所有离子的浓度都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三蝶烯是最初的“分子马达”的关键组件,三碟烯某衍生物X可用于制备吸附材料,其结构如图所示,3个苯环在空间上互为120°夹角。下列有关X的说法错误的是

A. 分子式为C22H14O4
B. 能发生加成、取代反应
C. 苯环上的一氯代物有3种
D. 分子中最多可能有20个原子位于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温时向2 L密闭容器中通入一定量的气体X和Y,发生反应:2X(g) + Y(g) ![]() 3Z(g),Y的物质的量n(Y)随时间t变化的曲线如图所示。下列说法正确的是
3Z(g),Y的物质的量n(Y)随时间t变化的曲线如图所示。下列说法正确的是
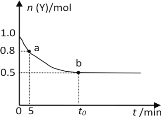
A.t0 min时,n(Z)=0.75 mol
B.0~5min内,以X表示的化学反应速率是0.02 mol·L-1·min-1
C.正反应速率a点比b点大
D.b点时该反应达到了最大限度,反应停止
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数小于36的X、Y、Z、R、W五种元素,其中X是周期表中原子半径最小的元素,Y是形成化合物种类最多的元素,Z原子基态时2p原子轨道上有3个未成对的电子,R单质占空气体积的![]() ;W的原子序数为29。回答下列问题:
;W的原子序数为29。回答下列问题:
(1)Y2X4分子中Y原子轨道的杂化类型为________,1mol Z2X4含有σ键的数目为 ________。
(2)化合物ZX3与化合物X2R的VSEPR构型相同,但立体构型不同,ZX3的立体构型为 ________,两种化合物分子中化学键的键角较小的是________(用分子式表示,下同)。
(3)与R同主族的三种非金属元素与X可形成结构相似的三种物质,试推测三者的稳定性由大到小的顺序________,理由是 ________;三者的沸点由高到低的顺序是 ________,解释原因________。
(4)元素Y的一种氧化物与元素Z的单质互为等电子体,元素Y的这种氧化物的分子式是________。
(5)W元素有________个运动状态不同的电子,其基态原子的价电子排布式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物1,,3,5,7-辛四烯可用于制合成纤维、染料、药物等,其结构 简式为![]() 。该物质的合成方法如下图所示:
。该物质的合成方法如下图所示:
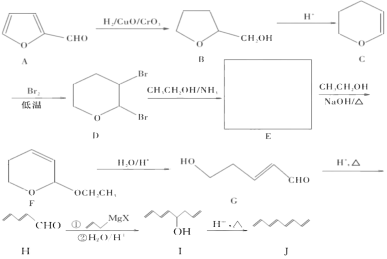
(1)1,3,5,7-辛四烯的分子式为______,有机物A所含含氧官能团有 _______(填名称)。
(2)E的结构简式为______.
(3)I→J的反应类型为______.
(4)![]() 在一定条件下可以发生加聚反应,合成无支链的链状有机高分子。写出该反应的化学方程式: ________________________ .
在一定条件下可以发生加聚反应,合成无支链的链状有机高分子。写出该反应的化学方程式: ________________________ .
(5)符合条件的G的同分异构体有___________种。
①与碳酸氢钠溶液反应产生气体 ②不能使溴水褪色
(6)以CH3CHO 、 HCHO和![]() 为原料也可以合成1,3,5,7-辛四烯,试写出合成路线。(其他试剂任选)_____________________________________________________________________ .已知:
为原料也可以合成1,3,5,7-辛四烯,试写出合成路线。(其他试剂任选)_____________________________________________________________________ .已知:![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
(1)写出反应的离子方程式_____________。
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号).
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用图中的曲线表示是________(填序号).

(4)若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应.则反应的离子方程式是 _________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 古人煮沸海水制取淡水,现代可通过向海水加入明矾实现海水淡化
B. 我国山水画所用的炭黑与“嫦娥四号”卫星所使用的碳纤维互为同分异构体
C. 某些筒装水使用的劣质塑料桶常含有乙二醇(![]() ),乙二醇不溶于水
),乙二醇不溶于水
D. “一带一路”是“丝绸之路经济带”和“21世纪海上丝绸之路”的简称,真丝绸的主要成分是蛋白质,属于天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸,又称草酸,通常在空气中易被氧化而变质。其两分子结晶水(H2C2O4·2H2O)却能在空气中稳定存在。在分析化学中常用H2C2O4·2H2O做KMnO4的滴定剂,下列关于H2C2O4的说法正确的是
A.草酸是二元弱酸,其电离方程式为H2C2O4![]() 2H++C2O
2H++C2O![]()
B.草酸滴定KMnO4属于中和滴定,可用石蕊做指示剂
C.乙二酸可通过乙烯经过加成、水解、氧化再氧化制得
D.将浓H2SO4滴加到乙二酸上使之脱水分解,分解产物是CO2和H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com