
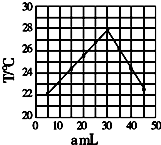
 将amL 0.1mol/LHCl溶液和bmL未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,实验结果如图(实验中始终保持a+b=50ml).下列叙述正确的是( )
将amL 0.1mol/LHCl溶液和bmL未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,实验结果如图(实验中始终保持a+b=50ml).下列叙述正确的是( )| A. | 做该实验时,环境温度为22摄氏度 | |
| B. | 该实验表明化学能可能转化为热能 | |
| C. | NaOH溶液的浓度约为0.1mol/L | |
| D. | 该实验表明有水生成的反应都是放热反应 |
分析 A.从图示观察起始温度即为实验时环境温度,为20℃;
B.根据图示所测溶液温度变化进行分析;
C.根据c酸V酸=c碱V碱进行计算;
D、实验只能证明该反应为放热反应.
解答 解:A.从图示观察起始温度即为实验时环境温度,因此该实验开始时温度是20℃,故A错误;
B.由图示可以看出该反应过程放出热量,表明化学能可能转化为热能,故B正确;
C、恰好反应时参加反应的盐酸体积为30mL,则碱的体积为20mL,c(NaOH)=$\frac{0.03L×0.1mol/L}{0.02L}$=0.15mol/L,故C错误;
D.此实验只能表明该反应为放热反应,其他有水生成的反应不一定为放热反应,故D错误,故选B.
点评 本题主要考查中和反应,侧重学生图象及中和实质的考查,训练学生观察分析问题的能力,以及利用化学方程式计算的能力,比较综合,要认真分析解答,题目难度不大.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
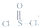 )中而形成的,电池总反应方程式为:4Li+2SOCl2=4LiCl+SO2+S,下列叙述中正确的是( )
)中而形成的,电池总反应方程式为:4Li+2SOCl2=4LiCl+SO2+S,下列叙述中正确的是( )| A. | 电解质溶液中混入水,对电池反应无影响 | |
| B. | 金属锂被还原,作电池的负极 | |
| C. | 电池工作过程中,Cl-向石墨电极移动 | |
| D. | 电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
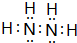 ,六个原子处在同一平面吗?否(是?否?).
,六个原子处在同一平面吗?否(是?否?).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
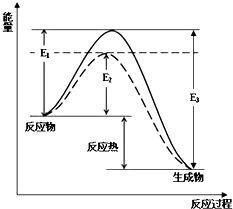 (1)工业合成氨是一个可逆反应:N2(g)+H2(g)?2NH3(g).图中虚线部分是通过改变化学反应中的条件,请解释原因:下表为不同温度下该反应的平衡常数.由此可推知,表中T1<573K(填“>”、“<”或“=”).
(1)工业合成氨是一个可逆反应:N2(g)+H2(g)?2NH3(g).图中虚线部分是通过改变化学反应中的条件,请解释原因:下表为不同温度下该反应的平衡常数.由此可推知,表中T1<573K(填“>”、“<”或“=”). | T/K | T1 | 573 | T3 |
| K | 1.00×107 | 2.54×105 | 1.88×103 |
| pH | <8.0 | 8.0~9.6 | >9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 灼烧CsCl时,火焰有特殊的颜色 | |
| B. | CsNO3易溶于水 | |
| C. | 在钠、钾、铯三种单质中,钠的熔点最低 | |
| D. | CsOH是弱碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
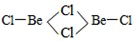
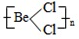
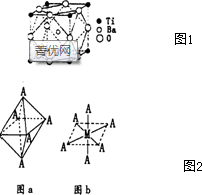
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
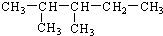 系统命名的名称为2,3-二甲基戊烷.
系统命名的名称为2,3-二甲基戊烷. .
.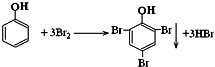 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com