
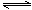 2C(g)+D(g) 已达平衡状态的是( )
2C(g)+D(g) 已达平衡状态的是( ) 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:不详 题型:单选题
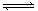 pC(g)达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍。下列说法中正确的是 ( )
pC(g)达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍。下列说法中正确的是 ( ) | A.m + n>p | B.平衡向正反应方向移动 |
| C. A的转化率降低 | D. C的体积分数增加 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g),平衡时C的体积分数与温度和压强的关系如图所示:
2C(g),平衡时C的体积分数与温度和压强的关系如图所示: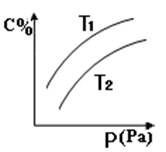 下
下| A.A一定为气体 | B.B一定为气体 |
| C.该反应是放热反应 | D.若正反应方向△H <0,则T1>T 2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2.5 mol | B.4.5 mol | C.5mol | D.7.5 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
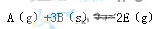 ,正反应放热。为使平衡状态向生成E的方向移动,适宜的条件是①高温、②低温、③高压、④低压、⑤加催化剂、⑥将E
,正反应放热。为使平衡状态向生成E的方向移动,适宜的条件是①高温、②低温、③高压、④低压、⑤加催化剂、⑥将E| A.①③⑥ | B.②③⑥ | C.②④⑥ | D.②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2C(g)+D(s);△H<0。
2C(g)+D(s);△H<0。
 (1)下列选项中,能表明甲和乙容器中反应一定达到平衡状态的是________。
(1)下列选项中,能表明甲和乙容器中反应一定达到平衡状态的是________。 测得C
测得C 的浓度为2 mol/L,此时容器的体积为________mL,B的转化率α甲(B)为________。
的浓度为2 mol/L,此时容器的体积为________mL,B的转化率α甲(B)为________。 达到平衡所需要的时间______2 min(填“>、<或=”),B的转化率α
达到平衡所需要的时间______2 min(填“>、<或=”),B的转化率α 乙(B) ______α甲(B) (填“>、<或=”)。
乙(B) ______α甲(B) (填“>、<或=”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
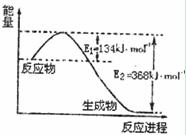
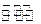 2NH3(g)
2NH3(g) 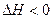
| t/℃ | 25 | 125 | 225 | … |
| K/(mol·L-1)-2 | 4.1×106 | K1 | K2 | … |
A.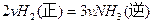 | B. |
| C.容器内压强保持不变 | D.混合气体的密度保持不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 △H=akJ/mol.
△H=akJ/mol. △H=bkJ/mol,
△H=bkJ/mol,| T/K | K1 | K2 | ||||
| 973 | 1.47 | 2.38 | ||||
| 1173 | 2.15 | 1.67
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |