
����Ŀ��ij��ȤС���ͬѧ������CCl4��ȡ��ˮ�еⵥ�ʣ�I2����ʵ��ʱ������������ζ�������ˮ�����ȫ��ɫ����Һ��������ͬѧ������ȡ���ˮ�л����еⵥ�ʣ�����ȡ������ȡʵ������Ч�����⣮
Ϊ̽��CCl4�Ե�ˮ�еⵥ�ʵ���ȡ�ʣ���С��ͬѧ����KI��Һ���Ƶ�ˮ������CCl4�Ըõ�ˮ�еⵥ�ʽ�����ȡ������ᴿI2��CCl4��Һ�е�I2���ڼ�����ȡ�ʣ�
��1����KI��������250ml 1mol/L KI��Һ������ȷ�IJ���˳���� ��
A����30mLˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
B������ƽȷ��ȡ�����KI����������������ˮ��Լ30mL�����ò������������裬ʹ�����ܽ�
C��������ȴ��KI��Һ�ز�����ע��250mL������ƿ��
D��������ƿ�ǽ����ߵ�ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�������
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶���1��2cm��
��2���������Ƶ���ҺŨ��ƫ�ߵ��� ��
A.����ǰ������ƿ������������ˮ
B.������ˮʱ���������˿̶���
C.����ʱ���ӿ̶���
D.������ƿ��ת����Һʱ������Һ����������ƿ����
��3������������KI��Һͨ������Cl2��ַ�����Ӧ��2KI+Cl2�TI2+2KCl�õ�I2��ˮ��Һ���������м���CCl4��ȡI2 �� ��Һ��ֲ���²���ҺΪɫ���õ��²���Һ�IJ����� ��
��4����ȡ��ʵ��С���ͬѧ�÷�Һ�ķ����õ�I2��CCl4��Һ�����ᴿ�õ�������I231.0g�����ʵ��CCl4����ȡ���� ��
���𰸡�
��1��B��C��A��F��E��D
��2��C
��3���Ϻ죻��Һ��ֲ����Һ©�����ϵIJ���������ʹ���ϵİ��ۣ���С�ף���©���ϵ�С�ף��ٽ���Һ©������Ļ���š����ʹ�²�Һ���������ձ�������
��4��97.6%
���������⣺��1�����Ʋ����Ǽ��㡢�������ܽ⡢ϴ�ӡ����ݡ�ҡ�ȡ�װƿ������ȷ�IJ���˳��B��C��A��F��E��D�����Դ��ǣ�B��C��A��F��E��D����2��A������ǰ������ƿ������������ˮ�������ʵ����ʵ�������Һ������������Ӱ�죬��Һ��Ũ�Ȳ����A��ѡ��B��������ˮʱ���������˿̶��ߣ�������Һ�����ƫ����Һ��Ũ��ƫ�ͣ��ʲ�ѡC������ʱ���ӿ̶��ߣ�������Һ�����ƫС����Һ��Ũ��ƫ�ͣ���ѡ��D��������ƿ��ת����Һʱ������Һ����������ƿ���棬�������ʵ����ʵ���ƫС����Һ��Ũ��ƫ�ͣ��ʲ�ѡ����ѡ��C����3��������������ǿ�ڵ⣬��������������KI��Һͨ������Cl2��ַ�����Ӧ��2KI+Cl2�TI2+2KCl�õ�I2��ˮ��Һ���������м���CCl4��ȡI2 �� ��Һ��ֲ���²���ҺΪ���Ϻ�ɫ���õ��²���Һ�IJ����ǣ���Һ��ֲ����Һ©�����ϵIJ���������ʹ���ϵİ��ۣ���С�ף���©���ϵ�С�ף��ٽ���Һ©������Ļ���š����ʹ�²�Һ���������ձ������£����Դ��ǣ��Ϻ죻��Һ��ֲ����Һ©�����ϵIJ���������ʹ���ϵİ��ۣ���С�ף���©���ϵ�С�ף��ٽ���Һ©������Ļ���š����ʹ�²�Һ���������ձ������£���4���⡢���Ȼ�̼��ܽ⣬���߷е㲻ͬ��ѡ��������룻250ml 1mol/L KI��Һ���е⻯�ص����ʵ���=0.25L��1mol/L=0.25mol�����ݷ���ʽ��2KI+Cl2�TI2+2KCl��֪���ɵ�0.125mol������Ϊ��0.125mol��254g/mol=31.75g��������ȡ�� ![]() ��100%=97.6%��
��100%=97.6%��
���Դ��ǣ�97.6%��
�����㾫������������һ�����ʵ���Ũ�ȵ���Һ�ǽ����ĸ�������Ҫ֪���������ʵ���Ũ����Һʱ�������ձ�������ˮ������ƿ�̶���1cm��2cm���ٸ��ý�Ͷ�ιܼ�ˮ���̶��ߣ�


 ����������ϵ�д�
����������ϵ�д� �Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
�Ż���ҵ�Ϻ��Ƽ����׳�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����
��1����98%��Ũ���ᣨ���ܶ�Ϊ1.84g/cm3������240mL1.0molL��1ϡ���ᣬ��ʵ�������У���Ͳ���ձ���������
��i������ȡŨ��������ΪmL��
��ii��ʵ��ʱ���õ��������� ��
��iii�����ƹ����У����������ʹ���ƽ��ƫ�ߵ���������ţ�
�ٳ���ʱ��������ƽ���̼����룬���̼��Ȼ��� ������ƿʹ��ʱδ����
�۶��ݺ���ҡ�ȡ����ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶���
����Һ��δϴ���ձ��Ͳ��������ݶ���ʱ���ӿ̶��߹۲�Һ��
��2�������28g KOH��������ܽ���gˮ�У�����ʹÿ108��ˮ��������1��K+ �� ������Һ���ܶ�Ϊ�� gcm��3 �� �����Һ��OH�������ʵ���Ũ��Ϊ �� ��������С�������λ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC4H7BrO2������̼�����Ʒ�Ӧ����������л�����Ŀ�������и�ѡ���л�����Ŀ��ͬ����(���������칹)
A. ����ʽΪC4H8O2���� B. ����ʽΪC5H10��ϩ��
C. �ױ���һ�ȴ��� D. ������( )�Ķ��ȴ���
)�Ķ��ȴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ڵȵ�������ǣ� ��
A.N2O4��NO2B.CH4��NH4+C.CO2��NO2D.C2H6��N2H6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��V LŨ��Ϊ0.5molL��1�����ᣬ��ʹ��Ũ������1������ȡ�Ĵ�ʩ�������ǣ� ��
A.ͨ���״���µ�HCl����11.2V L
B.����10 molL��1������0.1V L����ϡ����1.5V L
C.����Һ����Ũ����0.5V L
D.����V L 1.5 molL��1�������Ͼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ϡ���������·���ˮ�ⷴӦֻ����һ�ֲ������( )
A. ���� B. ������ C. ��֬ D. ��ѿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.�����仯����֮����ת��������ʽ��ʾ��
![]()
�ش������й����⣺
��1��������������Һ���Ƿ����Fe2+�ķ�����_____________________________________��
��2���ɷ��Ʊ��������Ƶ���Ҫ��ӦΪ2FeSO4+6Na2O2= 2Na2FeO4+2Na2O+2Na2SO4+O2��
�÷�Ӧ�е���������______________��ÿ����l mol Na2FeO4ת��_____________mol���ӡ�
��3��ʪ���Ʊ��������(K2FeO4)�ķ�Ӧ��ϵ������������
Fe(OH)3��ClO-��OH-��FeO42-��Cl-��H2O��
��д������ƽʪ���Ƹ�����ص����ӷ�Ӧ����ʽ��___________________________________��
������Ӧ������ת����0.3 mol���ӣ���ԭ��������ʵ���Ϊ______________________��
II.ij��ѧС��ͨ���������ϣ����������ͼ��ʾ�ķ����Ժ����ϴ���Ϊԭ�����Ʊ�NiSO4��7H2O����֪ij�������ĺ����ϴ�����Ҫ����Ni��������Al(31��)��Fe(1��3��)�ĵ��ʼ������������������(3.3��)��

����������������������ʽ����ʱ��pH���£�
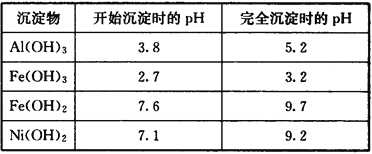
��1��������������з�����Ӧ��������_________________���ѧʽ����
��2���������ʱ����������� _________________ (�ѧʽ)��
��3������H2O2ʱ������Ӧ�����ӷ���ʽΪ_____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ö��Ե缫���������Һ����ʼʱ�������ϲ�������O2����
A. K2SO4��Һ B. HNO3��Һ C. NaI��Һ D. Ba(OH)2��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com