
| A、CH2═CH2 |
| B、SO2 |
| C、H2 |
| D、CH3-CH3 |
科目:高中化学 来源: 题型:
| A、含1molH2O的冰中含氢键数为2NA |
| B、12g金刚石中含有C-C键的个数为4NA |
| C、6g SiO2晶体中硅氧共价键数0.2NA |
| D、28gC2H4中含有的σ键为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验目的 | 实验设计 |
| A | 除去CO2中少量的SO2 | 将混合气体通过饱和Na2CO3溶液 |
| B | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硝酸 |
| C | 证明钠的金属活动性比铝强 | 向AlCl3溶液中投入金属钠 |
| D | 证明H2CO3酸性比H2SiO3强 | 将CO2通入Na2SiO3溶液中 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸 | B、盐酸 |
| C、氢氧化钠 | D、硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
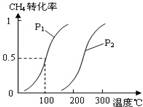 甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇.
甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇.| 实验编号 | (℃) | n (CO)/n(H2) | P(MPa) | ||
| ⅰ | 150 |
| 0.1 | ||
| ⅱ | 5 | ||||
| ⅲ | 350 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K3C60中只有离子键 |
| B、K3C60中碳元素显-3价 |
| C、该晶体在熔融状态下能导电 |
| D、C60与12C互为同素异形体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com