
 氨气是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用.
氨气是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用.| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |


科目:高中化学 来源: 题型:
| A、若X的反应速率为0.2 mol?L-1?s-1,则Z的反应速率为0.3 mol?L-1?s-1 |
| B、若向容器中充入氦气,压强增大,Y的转化率提高 |
| C、升高温度,正反应速率减小,平衡向逆反应方向移动 |
| D、开始充入容器中的X、Y物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯和浓硫酸在70~80℃时发生磺化反应 | ||
| B、芳香烃是分子组成符合CnH2n-6(n≥6)的一类物质 | ||
| C、甲苯可以和浓硝酸与浓硫酸的混合物发生硝化反应 | ||
D、等质量的烃(CXHY)耗氧量取决于
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,在银锌原电池中,以硫酸铜为电解质溶液,锌为
如图所示,在银锌原电池中,以硫酸铜为电解质溶液,锌为查看答案和解析>>
科目:高中化学 来源: 题型:
| 180℃ |
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
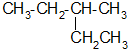 的系统命名为
的系统命名为 和一个-F,符合此要求的可能结构有
和一个-F,符合此要求的可能结构有查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com