
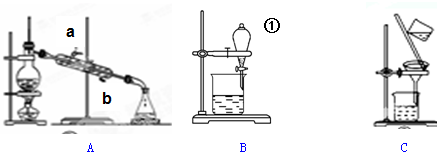
·ÖĪö £Ø1£©ÓĆ×°ÖĆA·ÖĄėCCl4ŗĶäå±½µÄ»ģŗĻĪļ£¬ĪŖÕōĮó£¬ĄäĖ®ĻĀ½ųÉĻ³ö£¬CCl4µÄ·Šµć·Ö±šĪŖ76.75”ę£»
£Ø2£©×°ÖĆBĪŖŻĶČ””¢·ÖŅŗ×°ÖĆ£¬ÓÉĶ¼æÉÖŖŅĒĘ÷µÄĆū³Ę£¬·ÖŅŗŹ±“ņæŖČū×ÓĄūÓĆĘųĢåµÄŃ¹Į¦Ź¹ŅŗĢåĖ³ĄūĮ÷ĻĀ£»
£Ø3£©Ń”ŌńNaOH³żČ„MgCl2£¬Ń”ŌńĀČ»Æ±µ³żČ„ĮņĖįŃĪ£¬Ń”ŌńĢ¼ĖįÄĘ³żČ„CaCl2£¬Ģ¼ĖįÄĘŅ»¶ØŌŚĀČ»Æ±µÖ®ŗó£¬æɳżČ„¹żĮæµÄ±µĄė×Ó£¬¹żĀĖŗó£¬×īŗóĻņĀĖŅŗÖŠ¼ÓŃĪĖį£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ£Ø1£©ÓĆ×°ÖĆA·ÖĄėCCl4ŗĶäå±½µÄ»ģŗĻĪļ£¬ĪŖÕōĮó£¬ŌŚŹµŃ鏱ĄäČ“Ė®“ÓĄäÄż¹ÜµÄb¶ĖĶØČė£¬CCl4µÄ·Šµć·Ö±šĪŖ76.75”ę£¬ŌņĪĀ¶Č¼Ę¶ĮŹżĪŖ80”ꏱ£¬×¶ŠĪĘæÖŠŹÕ¼Æµ½µÄĪļÖŹŹĒCCl4£¬¹Ź“š°øĪŖ£ŗb£»CCl4£»
£Ø2£©×°ÖĆBÖŠŅĒĘ÷¢ŁµÄĆū³ĘŹĒ·ÖŅŗĀ©¶·£¬ÓĆ×°ÖĆB·ÖĄė»ģŗĻĪļŹ±£¬ĪŖŹ¹ŅŗĢåĖ³ĄūĮ÷ĻĀ£¬Ó¦½ųŠŠµÄ²Ł×÷ŹĒ“ņæŖ·ÖŅŗĀ©¶·µÄČū×Ó£¬
¹Ź“š°øĪŖ£ŗ·ÖŅŗĀ©¶·£»“ņæŖ·ÖŅŗĀ©¶·µÄČū×Ó£»
£Ø3£©Ń”ŌńNaOH³żČ„MgCl2£¬Ń”ŌńĀČ»Æ±µ³żČ„ĮņĖįŃĪ£¬Ń”ŌńĢ¼ĖįÄĘ³żČ„CaCl2£¬Ģ¼ĖįÄĘŅ»¶ØŌŚĀČ»Æ±µÖ®ŗó£¬æɳżČ„¹żĮæµÄ±µĄė×Ó£¬¹żĀĖŗó£¬×īŗóĻņĀĖŅŗÖŠ¼ÓŃĪĖį£¬ŌņÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ¢Ż¢Ś¢Ū¢Ł¢Ž¢Ü¢ß»ņ¢Ż¢Ū¢Ś¢Ł¢Ž¢Ü¢ß£¬¹Ź“š°øĪŖ£ŗAD£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļ·ÖĄėĢį“棬ĪŖøßĘµæ¼µć£¬°ŃĪÕ»ģŗĻĪļ·ÖĄėĢį“æŹµŃ锢ŅĒĘ÷µÄŹ¹ÓĆĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėŹµŃéÄÜĮ¦µÄ漲飬עŅā·ÖĄėŹµŃé×°ÖĆ¼°“ÖŃĪĢį“棬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | V3£¾V2£¾V1 | B£® | V3=V2£¾V1 | C£® | V3£¾V2=V1 | D£® | V1=V2£¾V3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | MgCl2+Ba£ØOH£©2ØTBaCl2+Mg£ØOH£©2”ż | B£® | CO2+2NaOHØTNa2CO3+H2O | ||
| C£® | CaCO3 $\frac{\underline{\;øßĪĀ\;}}{\;}$CaO+CO2”ü | D£® | H2+CuO $\frac{\underline{\;\;”÷\;\;}}{\;}$H2O+Cu |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
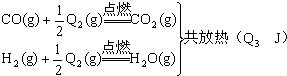
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŽÉ«ČÜŅŗŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±äĄ¶£»½įĀŪ£ŗČÜŅŗŅ»¶Ø³Ź¼īŠŌ | |
| B£® | ĪŽÉ«ČÜŅŗŃęÉ«·“Ó¦³Ź×ĻÉ«£ØĶø¹żĄ¶É«īܲ£Į§¹Ū²ģ£©£¬½įĀŪ£ŗČÜŅŗÖŠŅ»¶Øŗ¬ÓŠK+ | |
| C£® | ŌŚĪŽÉ«ČÜŅŗÖŠ¼ÓČėNa2CO3ČÜŅŗ²śÉś°×É«³Įµķ£»½įĀŪ£ŗČÜŅŗÖŠŅ»¶Øŗ¬ÓŠCa2+ | |
| D£® | ŌŚĪŽÉ«ŃĪČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬¼ÓČČ²śÉśµÄĘųĢåŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£»½įĀŪ£ŗČÜŅŗŅ»¶Øŗ¬ÓŠNH4+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ³£ĪĀ”¢³£Ń¹ĻĀ£¬11.2 L N2ŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.5NA | |
| B£® | ±ź×¼×“æöĻĀ£¬22.4 L H2ŗĶO2µÄ»ģŗĻĘųĢåĖłŗ¬·Ö×ÓŹżĪŖNA | |
| C£® | ŌŚ±ź×¼×“æöĻĀ£¬1 mol H2ŗĶ1 mol H2OĖłÕ¼µÄĢå»ż¶¼Ō¼ĪŖ22.4 L | |
| D£® | ±ź×¼×“æöĻĀ£¬1 mol CCl4µÄĢå»żŹĒ22.4 L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
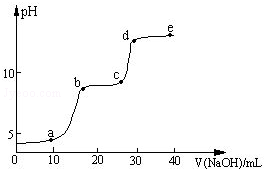
| ½Ļ“óĮæ“ęŌŚµÄŗ¬½šŹōŌŖĖŲµÄĄė×Ó | ¼ģŃé·½·Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ»š²ńµćČ¼¾Ę¾«µĘ | |
| B£® | ĻØĆš¾Ę¾«µĘ»šŃꏱ£¬ÓƵĘƱøĒĆš | |
| C£® | ÓĆ¾Ę¾«µĘĶāŃęøųĪļÖŹ¼ÓČČ | |
| D£® | ÓĆČ¼×ÅµÄ¾Ę¾«µĘČ„µćČ¼ĮķŅ»Õµ¾Ę¾«µĘ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com