



 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.都属于酸性氧化物,均能与水反应生成相应的酸 |
| B.大气中CO2的含量升高会引起“温室效应” |
| C.CO2具有较强的氧化性,同时也具有较强的还原性 |
| D.SiO2能与NaOH反应,也能与氢氟酸反应,所以SiO2是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
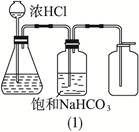

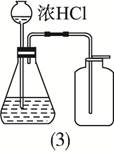
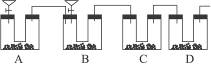
| A.(1)(2)(3)一样重 | B.(1)中最重 |
| C.(2)中最重 | D.(3)最轻 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
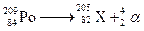 。对元素X的推断错误的是( )
。对元素X的推断错误的是( )| A.X原子核有6个电子层 | B.X的碳酸正盐不溶于水 |
| C.X的高价化合物比低价化合物稳定 | D.X是金属 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

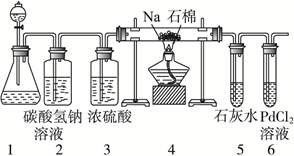
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
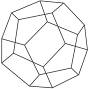
| A.C20与C60、C70互为同素异形体 | B.C20中有12个五边形,30条棱边 |
| C.C20具有很高的硬度和熔沸点 | D.C20的摩尔质量是240 g·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.自然界硅元素的贮量丰富 | B.硅可用于制造光导纤维 |
| C.高纯度的单质硅被广泛用于制作计算机芯片 | D.硅可由二氧化硅还原制得 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com