
【题目】硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等.
(1)新制的绿矾(FeSO47H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式: .
(2)已知FeSO4在不同条件下分解得到产物不同,可能是FeO和SO3 , 也可能是Fe2O3、SO3和SO2;SO3熔点是16.8℃,沸点是44.8℃.
某研究性学习小组拟用下列装置进行实验探究“在加热条件下FeSO4的分解产物”.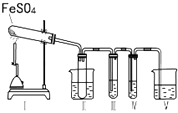
上述装置Ⅲ和Ⅳ用来检验气体产物.试回答下列问题:
①Ⅱ装置烧杯中水的温度应控制在(选填“0℃、25℃、50℃”),装置Ⅱ的作用是 .
②装置Ⅲ中的试剂可以是(选填序号,下同),现象是 , 则证明气体产物中含有SO3; 装置Ⅳ中的试剂可以是 .
A.2mol/LNa2CO3溶液 B.品红溶液
C.0.5mol/L BaCl2溶液 D.0.5mol/LBa(NO3)2
E.0.01mol/L KMnO4溶液 F.淀粉碘化钾溶液
③装置V中试剂为NaOH溶液,发生反应的离子方程式为 .
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
操作步骤 | 预期实验现象 | 预期实验结论 |
向其中一份溶液中加入 | 固体中含有Fe2O3 | |
向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液 | 产生蓝色沉淀 |
⑤若用22.8g FeSO4固体做实验,完全分解后,得到11.2g固体,其中Fe2O3的质量分数=
(精确到0.1%)
【答案】
(1)4FeSO4?7H2O+O2=4Fe(OH)SO4+26H2O
(2)50℃;防止产生倒吸;C;产生白色沉淀;BE;SO2+2OH﹣=SO32﹣+H2O;KSCN溶液;溶液变成血红色;固体中含有FeO;35.7%
【解析】解:(1)亚铁离子具有还原性,易被氧气氧化,反应方程式为:4FeSO47H2O+O2=4Fe(OH)SO4+26H2O,所以答案是:4FeSO47H2O+O2=4Fe(OH)SO4+26H2O;(2)①SO3的沸点是44.8°C,当温度高于44.8°C时三氧化硫为气体状态,把试管浸泡在50℃的热水浴中能防止SO3液化或凝固,产生的气体极易和溶液反应时,会产生倒吸,所以装置II的试管能防止溶液倒吸入装置Ⅰ中(或安全瓶),所以答案是:50℃;防止产生倒吸:②装置III是检验是否有三氧化硫,可以选用氯化钡溶液,如果有白色沉淀生成说明有三氧化硫;装置IV是检验是否有二氧化硫,二氧化硫能使品红褪色,也能使酸性高锰酸钾溶液褪色,所以可以选用二者来检验二氧化硫;所以答案是:C;产生白色沉淀;B、E;③二氧化硫会污染空气,所以要用氢氧化钠溶液来吸收剩余的二氧化硫,其反应的离子方程式为:SO2+2OH﹣=SO32﹣+H2O,所以答案是:SO2+2OH﹣=SO32﹣+H2O;④检验三价铁离子用硫氰化钾溶液,溶液变红色,证明有三价铁离子,进而说明固体产物中含有氧化铁;检验二价铁离子用K3[Fe(CN)6]溶液,溶液中生成蓝色沉淀,说明有二价铁离子,即证明固体产物中含有FeO;所以答案是:
操作步骤 | 预期实验现象 | 预期实验结论 |
KSCN溶液(或硫氰化钾溶液) | 溶液变成血红色 | |
固体中含有FeO |
⑤反应过程中FeSO4固体分解为二氧化硫、三氧化硫、FeO、Fe2O3 , 完全分解后得到11.2g固体为氧化铁和氧化亚铁,质量减少的为二氧化硫和三氧化硫的总质量,设生成的二氧化硫为xmol,三氧化硫为ymol,根据硫元素守恒,则x+y= ![]() =0.15mol, 64x+80y=22.8g﹣11.2g=11.6g,解得:x=0.025,y=0.125, FeSO4固体分解,每生成1mol二氧化硫时硫元素得到2mol电子,每生成1molFe2O3时铁元素失去2mol电子,所以生成的二氧化硫与氧化铁的物质的量相同,则Fe2O3的物质的量为0.025mol,其质量为0.025mol×160g/mol=4.0g,故质量分数为:
=0.15mol, 64x+80y=22.8g﹣11.2g=11.6g,解得:x=0.025,y=0.125, FeSO4固体分解,每生成1mol二氧化硫时硫元素得到2mol电子,每生成1molFe2O3时铁元素失去2mol电子,所以生成的二氧化硫与氧化铁的物质的量相同,则Fe2O3的物质的量为0.025mol,其质量为0.025mol×160g/mol=4.0g,故质量分数为: ![]() ×100%=35.7%,所以答案是:35.7%.
×100%=35.7%,所以答案是:35.7%.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】下列仪器:①漏斗、②容量瓶、③蒸馏烧瓶、④坩埚、⑤分液漏斗、⑥燃烧匙,常用于物质分离的是
A. ①③④ B. ①②⑥ C. ①③⑤ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乙醇、糖类和蛋白质都是人体必需的营养物质
B. 淀粉和纤维素都可以作为工业上生产葡萄糖的原料
C. 蔗糖、果糖的分子式均为C6H12O6,二者互为同分异构体
D. 纤维素和淀粉均属于糖类,它们在人体内水解的最终产物均为葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气、煤炭气(CO、H2)的研究在世界上相当普遍。其中天然气和二氧化碳可合成二甲醚,二甲醚与水蒸气制氢气作为燃料电池的氢能源,比其他制氢技术更有优势.主要反应为:
①CH3OCH3(g)+H2O(g)2CH3OH(g);△H=37kJmol-1
②CH3OH(g)+H2O(g)3H2(g)+CO2(g);△H=49kJmol-1
③CO2(g)+H2(g)CO(g)+H2O(g);△H=41.3kJmol-1
其中反应③是主要的副反应,产生的CO对燃料电池Pt电极有不利影响.
请回答下列问题:
(1)二甲醚可以通过天然气和CO2合成制得,该反应的化学方程式为______________.
(2)CH3OCH3(g)与水蒸气制氢气的热化学方程式为______________.
(3)下列采取的措施和解释正确的是______________(填字母).
A.反应过程在低温进行,可减少CO的产生
B.增加进水量,有利于二甲醚的转化,并减少CO的产生
C.选择在高温具有较高活性的催化剂,有助于提高反应②CH3OH的转化率
D.体系压强升高,虽然对制取氢气不利,但能减少CO的产生
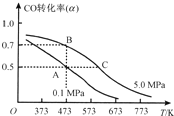
(4)煤炭气在一定条件下可合成燃料电池的另一种重要原料甲醇,反应的化学方程式为CO(g)+2H2(g)CH3OH(g);△H<0.现将10molCO与20molH2置于密闭容器中,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(α)与温度、压强的关系如图所示.
①自反应开始到达平衡状态所需的时间tA________tB(填“大于”“小于”或“等于”).
②A、C两点的平衡常数KA____KC(填“大于”“小于”或“等于”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和生活中有着广泛的应用,下列说法不正确的是
A. 二氧化硫具有漂白性,可广泛用于食品的增白
B. 鉴别蚕丝和人造丝(纤维素)的方法之一是灼烧,有烧焦羽毛气味的是蚕丝
C. 农村兴建沼气池将秸秆发酵产生沼气,可减少因焚烧带来的环境污染
D. 用浸泡过高锰酸钾溶液的硅藻土吸收水果产生的乙烯可达到保鲜的目的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com