
【题目】在100克浓度为18mol/L.密度为ρ(g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加水的体积为(提示:硫酸溶液越浓,其密度越大)
A. 小于100mL B. 等于100mL
C. 大于100mL D. 无法确定
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的自然科学. 某同学需要配制0.1molL﹣1 的NaHCO3溶液500mL,请根据溶液配制过程中的情况回答下列问题:
(1)NaHCO3的俗称;配制0.1molL﹣1 的NaHCO3溶液时,应称取固体NaHCO3的质量为 .
(2)实验中除了托盘天平(带砝码和镊子)、烧杯、药匙、玻璃棒外还需要的其它仪器有;其中两次用到玻璃棒,其作用分别是 .
(3)定容观察液面时俯视刻度线,所配溶液浓度(填“偏高”、“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关对该溶液的判断不正确的是( ) 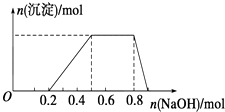
A.该溶液中肯定含有的离子是H+、NH4+、Al3+、SO42﹣
B.肯定不含的阳离子是Mg2+、Fe3+
C.要确定该溶液是否含有Na+ , 必须做焰色反应实验,看焰色是否为黄色
D.该溶液中肯定含有的离子的物质的量之比为n(H+):n(NH4+):n(Al3+):n(SO42﹣)=2:3:1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁(已知炽热铁屑与氯化氢生成氯化亚铁).现用如图所示的装置模拟上述过程进行试验. 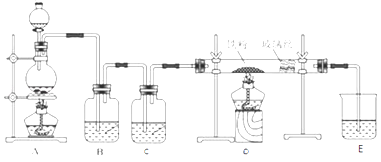
回答下列问题:
(1)盛装浓盐酸的仪器名称为 , 进行实验时,应先点燃(选填A或C)处酒精灯,装置B中加入的试剂是 , 装置C中加入的试剂 , 检验FeCl3的常用试剂为 .
(2)制取无水氯化铁的实验中,A中反应的离子方程式为 .
(3)若无B装置,反应尾气成分为 , 用E装置吸收尾气可能存在的问题、
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知核电荷数均小于18的X、Y、Z、W四种元素原子的电子层数相同,而原子半径依次增大,则下列物质中酸性最强的是( )
A. HXO4B. H2YO4C. H3ZO4D. H4WO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若室温时0.1mol/L的盐NaR的溶液的PH=10,0.1mol/L的酸HR的溶液PH=3,则两种溶液中水的电离度的比值是
A.1:104B.1:1C.1:10-7D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)机智如化学老师的你用固体烧碱配制500mL0.20molL﹣1的NaOH溶液,需要称取g固体,定容时除了胶头滴管和玻璃棒,还需要的仪器为 .
(2)语文老师要用36.5%(ρ=1.18gcm﹣3 )的浓盐酸配制0.4molL﹣1的盐酸240mL,需准确量取36.5%的浓盐酸mL.
(3)若配制0.5molL﹣1的硫酸溶液的其他操作均正确,但出现下列错误操作,下列所配制的硫酸溶液浓度偏低的是(填序号).
A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒.
B.移液时容量瓶中有少量蒸馏水.
C.用胶头滴管向容量瓶中加水时溶液凹面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切.
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切.
E.稀释后没冷却到室温就将溶液转移至容量瓶.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com