
”¾ĢāÄæ”æĻĀĮŠŹōÓŚ¼īŠŌŃõ»ÆĪļµÄŹĒ£Ø £©
A.SiO2B.Na2O
C.Na2O2D.NaOH

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹÆÓĶŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬æÉÉś²śĘūÓĶ”¢ĆŗÓĶ”¢ŅŅĻ©”¢±½µČ£¬ŹµĻÖŹÆÓĶµÄ ×ŪŗĻĄūÓĆ£¬¼õÉŁ»·¾³ĪŪČ¾£¬ŹĒČĖĄąĆęĮŁµÄÖŲ“óæĪĢā£®
£Ø1£©½«ŹÆÓĶ·ÖĮó»ńµĆĘūÓĶ”¢ĆŗÓĶµČĒįÖŹÓĶ£¬ŹĒĄūÓĆĮĖø÷×é·ÖµÄ_________²»Ķ¬£»½« ÖŲÓĶĮŃ½āæÉŅŌ»ńµĆŗܶą»Æ¹¤ŌĮĻ£¬Čē C8C18![]() C4H10+_____£»
C4H10+_____£»
£Ø2£©ŅŅĻ©æÉÖĘČ”¾ŪŅŅĻ©ĖÜĮĻ£¬¾ŪŅŅĻ©µÄ½į¹¹¼ņŹ½ŹĒ______ £¬ĖüŹōÓŚøß·Ö×Ó ²ÄĮĻ£¬“óĮæŹ¹ÓĆĖÜĮĻČŻŅ×Ōģ³ÉµÄ»·¾³ĪŹĢāŹĒ_______£»
£Ø3Ęū³µĪ²ĘųÖŠµÄ NO ŹĒĪķö²³ÉŅņÖ®Ņ»£¬ÖĪĄķĖüµÄŅ»ÖÖ·½·ØŹĒŌŚ 400”ę”¢“߻ƼĮ“ęŌŚµÄĢõ¼žĻĀŹ¹ NO Óė NH3 ·“Ӧɜ³É¶Ō“óĘųĪŽĪŪČ¾µÄĪļÖŹ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ__________________£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚŌŖĖŲW”¢X”¢Y”¢ZµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĒŅY”¢ZĪ»ÓŚĶ¬ÖÜĘŚ”£¼×”¢ŅŅ”¢¼ŗŹĒÓÉÕāŠ©ŌŖĖŲ×é³ÉµÄ¶žŌŖ»ÆŗĻĪļ”£ 0.001 molL-1 µÄ¼ŗČÜŅŗpHĪŖ3£»øżŹĒ¾ßÓŠĘư׊ŌµÄ»ģŗĻĪļ”£ÉĻŹöĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£ŗ£Ø £©

A. Ō×Ó°ė¾¶Z£¾Y£¾X
B. ½öÓÉÕāĖÄÖÖŌŖĖŲ¹¹³ÉµÄČÜŅŗæÉÄܳŹĖįŠŌ”¢¼īŠŌ»ņÖŠŠŌ
C. ¼ŗĪŖÓɼ«ŠŌ¼ü¹¹³ÉµÄ·Ē¼«ŠŌ·Ö×Ó
D. ĪģĪŖŅ»ŌŖČõ¼ī
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§Ņņø¹ŠŗŅżĘšÉķĢåŃĻÖŲȱĖ®£¬Ņ½Éś³ż¶ŌĘä½ųŠŠŅ©ĪļÖĪĮĘĶā»¹æ¼ĀĒ²¹Ņŗ£¬ĻĀĮŠ²¹Ņŗ·½·Ø×īŗĻĄķµÄŹĒ£Ø £©
A.ŗČĘĻĢŃĢĒĖ®B.ŗČĻŹ³ČÖ
C.ŹäÉśĄķŃĪĖ®D.ŹäÕōĮóĖ®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijæĘѧŠ”×éÖʱøĻõ»ł±½µÄŹµŃé×°ÖĆČēĻĀ£¬ÓŠ¹ŲŹż¾ŻĮŠČēĻĀ±ķ”£ŅŃÖŖ“ęŌŚµÄÖ÷ŅŖø±·“Ó¦ÓŠ£ŗŌŚĪĀ¶ČÉŌøßµÄĒéæöĻĀ»įÉś³É¼ä¶žĻõ»ł±½”£

ŹµŃé²½ÖčČēĻĀ£ŗ
Č”100mLÉÕ±£¬ÓĆ20 mLÅØĮņĖįÓė×ćĮæÅØĻõĖįÅäÖĘ»ģŗĶĖį£¬½«»ģŗĻĖįŠ”ŠÄ¼ÓČėBÖŠ”£°Ń18 mL£Ø15£®84 g£©±½¼ÓČėAÖŠ”£ĻņŹŅĪĀĻĀµÄ±½ÖŠÖšµĪ¼ÓČė»ģĖį£¬±ßµĪ±ß½Į°č£¬»ģŗĶ¾łŌČ”£ŌŚ50”«60”ęĻĀ·¢Éś·“Ó¦£¬Ö±ÖĮ·“Ó¦½įŹų”£
½«·“Ó¦ŅŗĄäČ“ÖĮŹŅĪĀŗóµ¹Čė·ÖŅŗĀ©¶·ÖŠ£¬ŅĄ“ĪÓĆÉŁĮæĖ®”¢5£„NaOHČÜŅŗŗĶĖ®Ļ“µÓ”£·Ö³öµÄ²śĪļ¼ÓČėĪŽĖ®CaCl2æÅĮ££¬¾²ÖĆʬæĢ£¬ĘśČ„CaCl2£¬½ųŠŠÕōĮó“æ»Æ£¬ŹÕ¼Æ205”«210”ęĮó·Ö£¬µĆµ½“æĻõ»ł±½18g”£
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ķ¼ÖŠ×°ÖĆCµÄ×÷ÓĆŹĒ____________________”£
£Ø2£©ÖʱøĻõ»ł±½µÄ»Æѧ·½³ĢŹ½_____________________”£
£Ø3£©ÅäÖĘ»ģŗĻĖįŹ±£¬ÄÜ·ń½«ÅØĻõĖį¼ÓČėµ½ÅØĮņĖįÖŠ_________£Ø”°ŹĒ”±»ņ”°·ń”±£©£¬ĖµĆ÷ĄķÓÉ£ŗ____________________”£
£Ø4£©ĪŖĮĖŹ¹·“Ó¦ŌŚ50”ꔫ60”ęĻĀ½ųŠŠ£¬³£ÓƵķ½·ØŹĒ______________”£·“Ó¦½įŹų²¢ĄäČ“ÖĮŹŅĪĀŗóAÖŠŅŗĢå¾ĶŹĒ“ÖĻõ»ł±½£¬“ÖĻõ»ł±½³Ź»ĘÉ«µÄŌŅņŹĒ_____________________”£
£Ø5£©ŌŚĻ“µÓ²Ł×÷ÖŠ£¬µŚ¶ž“ĪĖ®Ļ“µÄ×÷ÓĆŹĒ_____________________”£
£Ø6£©ŌŚÕōĮó“æ»Æ¹ż³ĢÖŠ£¬ŅņĻõ»ł±½µÄ·ŠµćøßÓŚ140”ę£¬Ó¦Ń”ÓĆæÕĘųĄäÄż¹Ü£¬²»Ń”ÓĆĖ®Ö±ŠĪĄäÄż¹ÜµÄŌŅņŹĒ_______________________”£
£Ø7£©±¾ŹµŃéĖłµĆµ½µÄĻõ»ł±½²śĀŹŹĒ_____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ¶žŃõ»ÆĢ¼ŗĶĒāĘųŌŚŅ»¶ØĢõ¼žĻĀæÉŅŌŗĻ³É¼×“¼£¬ĘäÖʱø·“Ó¦ĪŖ£ŗCO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£ŗ
CH3OH(g)+H2O(g) ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£ŗ
A. µ÷æŲ·“Ó¦Ģõ¼ž²»ÄÜøı䷓ӦĻŽ¶Č
B. »Æѧ·“Ó¦µÄĻŽ¶Č¾ö¶ØĮĖ·“Ó¦ĪļŌŚøĆĢõ¼žĻĀµÄ×ī“ó×Ŗ»ÆĀŹ
C. µ±CO2µÄĻūŗÄĖŁĀŹµČÓŚĘäÉś³ÉĖŁĀŹŹ±£¬øĆ·“Ó¦ŅŃĶ£Ö¹
D. Ķ¶Čė3molH2ÄܵƵ½1molµÄCH3OH
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ“Óŗ£Ė®ÖŠæÉŅŌĢįČ”ŗܶąÓŠÓƵÄĪļÖŹ£¬ĄżČē“Óŗ£Ė®ÖĘŃĪĖłµĆµ½µÄĀ±Ė®ÖŠæÉŅŌĢįČ”µā”£»īŠŌĢæĪüø½·ØŹĒ¹¤ŅµĢįµāµÄ·½·ØÖ®Ņ»£¬ĘäĮ÷³ĢČēĻĀ£ŗ

׏ĮĻĻŌŹ¾£ŗ¢ń£®pH=2Ź±£¬NaNO2ČÜŅŗÖ»Äܽ«I-Ńõ»ÆĪŖI2,Ķ¬Ź±Éś³ÉNO£»
¢ņ£®I2+5Cl2+6H2O=2HIO3+10HCl£»
¢ó£®5SO32-+2IO3-+2H+=I2+5SO42-+H2O£»
¢ō£®I2ŌŚ¼īŠŌČÜŅŗÖŠ·“Ӧɜ³ÉI-ŗĶIO3-”£
(1)·“Ó¦¢ŁµÄĄė×Ó·½³ĢŹ½_____________”£
(2)·½°ø¼×ÖŠ£¬øł¾ŻI2µÄĢŲŠŌ£¬·ÖĄė²Ł×÷XµÄĆū³ĘŹĒ________________”£
(3)ŅŃÖŖ£ŗ·“Ó¦¢ŚÖŠĆæĪüŹÕ3molI2×ŖŅĘ5molµē×Ó£¬ĘäĄė×Ó·½³ĢŹ½ŹĒ_______________”£
(4)Cl2”¢ĖįŠŌKMnO4µČ¶¼ŹĒ³£ÓƵÄĒæŃõ»Æ¼Į£¬µ«øĆ¹¤ŅÕÖŠŃõ»ÆĀ±Ė®ÖŠµÄI-Č“Ń”ŌńĮĖ¼Ūøń½ĻøßµÄNaNO2,ŌŅņŹĒ_______________”£
(5)·½°øŅŅÖŠ£¬ŅŃÖŖ·“Ó¦¢Ū¹żĀĖŗó£¬ĀĖŅŗÖŠČŌ“ęŌŚÉŁĮæµÄI2”¢I-”¢IO3-”£Ēė·Ö±š¼ģŃéĀĖŅŗÖŠµÄI-”¢IO3-£¬½«ŹµŃé·½°ø²¹³äĶźÕū”£ŹµŃéÖŠæɹ©Ń”ŌńµÄŹŌ¼Į£ŗĻ”H2SO4”¢µķ·ŪČÜŅŗ”¢Fe2(SO4)3ČÜŅŗ”¢Na2SO3ČÜŅŗ
A£®ĀĖŅŗÓĆCCl4¶ą“ĪŻĶČ””¢·ÖŅŗ£¬Ö±µ½Ė®²ćÓƵķ·ŪČÜŅŗ¼ģŃé²»³öµāµ„ÖŹ“ęŌŚ”£
B£®_______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĪļÖŹ½į¹¹ŃŠ¾æµÄĄśŹ·ÉĻ£¬Ź×ĻČĢį³öŌ×ÓÄŚÓŠµē×ÓѧĖµµÄŹĒ£Ø £©
A. µĄ¶ū¶Ł B. Ā¬ÉŖø£ C. ĢĄÄ·Éś D. ²Ø¶ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻ³£ŅŌøõĢśæó(Ö÷ŅŖ³É·ÖĪŖŃĒøõĖįŃĒĢśFeCr2O4£¬»¹ÓŠAl2O3”¢SiO2µČŌÓÖŹ)ĪŖÖ÷ŅŖŌĮĻÉś²śŗģ·ÆÄĘ(Na2Cr2O7)£¬Ä³ŹµŃ銔×éÄ£ÄāĘäĮ÷³ĢČēĻĀĶ¼ĖłŹ¾£ŗ
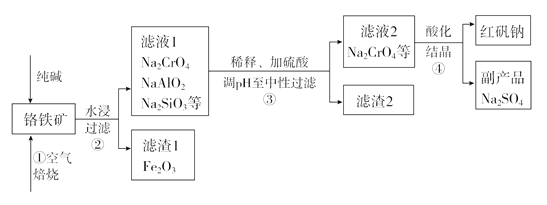
£Ø1£©²½Öč¢ŁÖŠ£¬±ŗÉÕŹ±ĖłÓƵÄŅĒĘ÷²Ä֏ӦєÓĆ_______(Ģī”°“ÉÖŹ”±”¢”°ĢśÖŹ”±»ņ”°ŹÆÓ¢ÖŹ”±)£¬¶žŃõ»Æ¹čÓė“æ¼ī·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___________”£
£Ø2£©ÅäĘ½²½Öč¢ŁÖŠÖ÷ŅŖ·“Ó¦£ŗ_________
____FeCr2O4£«___O2£«___Na2CO3![]() ___Fe2O3£«___Na2CrO4£«___CO2
___Fe2O3£«___Na2CrO4£«___CO2
£Ø3£©²Ł×÷¢ÜÖŠ£¬Ėį»ÆŹ±£¬CrO42£×Ŗ»ÆĪŖCr2O72££¬Š“³öĘ½ŗā×Ŗ»ÆµÄĄė×Ó·½³ĢŹ½£ŗ______________”£
£Ø4£©²½Öč¢ŪÓĆĮņĖį½«ČÜŅŗµÄpHµ÷ÖĮÖŠŠŌ£¬ĖłµĆĀĖŌüµÄÖ÷ŅŖ³É·ÖŹĒ___________”¢____________£»
£Ø5£©ĻĀĶ¼ŹĒNa2Cr2O7”¤2H2OŗĶNa2SO4µÄČܽā¶ČĒśĻߣ¬²½Öč¢ÜÖŠ»ńµĆ¹ĢĢ¬ø±²śĘ·Na2SO4µÄŹµŃé²Ł×÷·½·ØĪŖ____________”¢___________”£
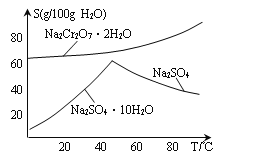
£Ø6£©¹¤ŅµÉĻ³£ÓƵē½ā·Ø“¦Ąķŗ¬Cr2O72£µÄĖįŠŌ·ĻĖ®£¬ÓĆ½šŹōĢś×÷Ńō¼«”¢ŹÆÄ«×÷Ņõ¼«£¬Ņ»¶ĪŹ±¼äŗó²śÉśFe(OH)3ŗĶCr(OH)3³Įµķ”£Čōµē½āŗóČÜŅŗÖŠc(Cr3+)=3.0”Į10£5mol”¤L£1£¬Ōņc(Fe3+)=_____”£(ŅŃÖŖKsp[Fe(OH)3]=4.0”Į10£38mol”¤L£1£¬Ksp[Cr(OH)3]=6.0”Į10£31mol”¤L£1)
£Ø7£©CrO5µÄ½į¹¹Ź½ĪŖ £¬øĆŃõ»ÆĪļÖŠCrĪŖ_______¼Ū”£
£¬øĆŃõ»ÆĪļÖŠCrĪŖ_______¼Ū”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com