
【题目】对应下列叙述的微粒M和N,肯定属于同主族元素且化学性质相似的是( )
A.原子核外电子排布式:M为1s22s2,N为1s2
B.结构示意图:M![]() ,N
,N![]()
C.M原子基态2p轨道上有一对成对电子,N原子基态3p轨道上有一对成对电子
D.M原子基态2p轨道上有1个未成对电子,N原子基态3p轨道上有1个未成对电子
【答案】C
【解析】
A. M核外电子排布式为:1s22s2,则M为Be,N核外电子排布式为:1s2,则为He,不是同主族元素,故A错误;
B. 根据核电荷数可知M为Ne,N为Na+,不是同主族元素,故B错误;
C. M原子基态2p轨道上有一对成对电子,则其核外电子排布式为:1s22s22p4,为O元素,N原子基态3p轨道上有一对成对电子,则其核外电子排布式为:1s22s22p63s23p4,为S元素,二者为同主族元素,化学性质相似,故C正确;
D. M原子基态2p轨道上有1个未成对电子,M可能为B或F元素,N原子基态3p轨道上有1个未成对电子,N可能为Al或Cl元素,所以M和N可能不属于同一族,故D错误;
故答案为C。


科目:高中化学 来源: 题型:
【题目】中国第二化工设计院提出,用间接电化学法对大气污染物 NO 进行无害化处理,其原理示意如图(质子膜允许H+和 H2O 通过),下列相关判断正确的是
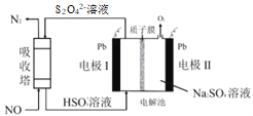
A.电极Ⅰ为阴极,电极反应式为 2H2O+2e- =2OH- +H2↑
B.电解池中质子从电极Ⅰ向电极Ⅱ作定向移动
C.吸收塔中的反应为 2NO+ 2S2O42-+H2O=N2+4HSO3-
D.每处理1molNO电解池质量减少16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法错误的是( )
A.密闭容器中,2molSO2和1molO2催化反应后分子总数大于2NA
B.1LpH=2的H2SO3溶液中含H+的数目为0.01NA
C.5.6g铁与稀硝酸反应生成0.08molNO,转移电子数为0.3NA
D.6.4 g S2和S8的混合物中所含硫原子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2又名黑锰矿,主要用于生产优质软磁铁氧体。MnO2的合成方法按制备工艺中所用原料的不同,分为固相合成和液相合成。已知:MnO2不溶于水,其中锰的价态有+2价,也可能有+3价和+4价。请回答下列问题:
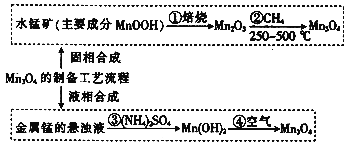
(1)若Mn3O4中锰的价态看作由+2和+4价组成,写出它由氧化物形成的表达式:_____
(2)MnOOH中锰的价态为________价,写出②的化学方程式:____;碱性锌锰干电池的电池反应为:Zn+2MnO2 + 2H2O=Zn(OH)2 + 2MnOOH,写出该电池正极的电极反应式______
(3)将(NH4)2SO4溶于水使锰的悬浊液显酸性,随即缓慢地产生气泡,试用相应的离子方程式解释原因____________。过滤出的Mn(OH)2需要洗涤,简要说明洗涤沉淀的操作过程:________。
(4)若③中收集到672mL(标准状况下)的H2,则理论上可以得到_________g Mn3O4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯氧化铋(BiOCl)常用于电子设备等领域,BiOCl难溶于水,它是BiCl3的水解产物。以铋的废料(主要含铋的化合物,含少量铜、铅、锌的硫酸盐及Cu2S和Fe2O3等)为原料生产高纯度BiOCl的工艺流程如下:
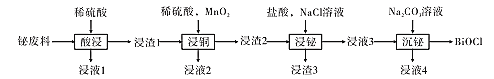
请回答下列问题:
(1)在浸液1中加入过量的锌,过滤,将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥得结晶水合物M,M的摩尔质量为287 g·mol-1,M为 ___(填化学式)。
(2)已知:浸液2呈蓝色,浸渣2含有少量硫单质。“浸铜”中MnO2的作用是____(用离子方程式表示)。
(3)“浸铋”中,铋的浸出率与温度关系如图所示:
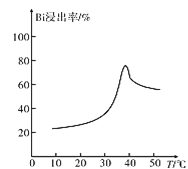
在高于40℃左右时“铋浸出率”开始下降,其主要因素可能是____(从两个角度分析)。
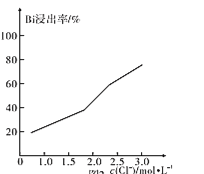
(4)在室温和液固比固定的条件下,c(HCl)=1.0mol·L-1时,铋的浸出率与溶液中c(Cl-)的关系如图所示。“浸铋”操作中,加入NaCl的目的是____。
(5)浸液3中主要溶质是BiCl3,“沉铋”过程中,有气体放出。“沉铋”的主要化学反应的方程式为____。从绿色化学角度看,浸液4可以用于____(填“酸浸”、“浸铜”或“浸铋”)。
(6)测定产品的纯度:取mg充分洗涤并干燥后的产品,溶于稍过量的浓硝酸中,加水稀释到100.0mL,取20.0mL于烧杯中,用cmol·L-1的AgNO3标准溶液滴定至终点(用Na2CrO4,作指示剂),消耗AgNO3标准溶液VmL,则产品中BiOCl的质量分数为____%(用含m、c、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在生产、生活中有广泛应用。回答下列问题:
(1)铜和锌相邻,铜和锌的几种状态:①铜:[Ar]3d10;②铜:[Ar]3d104s1③铜:[Ar]3d104p1④锌:[Ar]3d104s1⑤锌:[Ar]3d104s2。它们都失去1个电子时需要的能量由大到小排序为 ___(填字母)。
a.①⑤④②③ b.①④⑤②③ c.②①③⑤④ d.⑤①④③②
画出基态铜原子的价电子排布图____。
(2)Cu2+与NH3·H2O等形成配离子。[Cu(NH3)4]2+中2个NH3被2个H2O取代得到两种结构的配离子,则[Cu(NH3)4]2+的空间构型是____(填“正四面体”或“正四边形”)。
(3)CuF2晶体的熔点为836℃。其能量循环图示如下(a、b、c 等均大于0):

F-F键能为 ___kJmol-1,CuF2(s)的晶格能为 ___kJmol-1。
(4)铜常作醇氧化反应的催化剂。M中C原子的杂化类型有 ___种,M的熔沸点比N的高,原因是 ___。
![]()
![]()
![]()
(5)磷青铜晶胞结构如图所示。NA代表阿伏加德罗常数的值,铜、磷原子最近距离为![]()
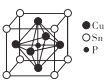
①铜与铜原子最近距离为____nm。
②磷青铜晶体密度为___ gcm-3(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2的结构可以表示为 ,CO的结构可以表示为
,CO的结构可以表示为 ,其中椭圆框表示 π键,下列说法不正确的是( )
,其中椭圆框表示 π键,下列说法不正确的是( )
A.N2 分子与 CO 分子中都含有三键
B.CO 分子中有一个 π 键是配位键
C.N2 与 CO 互为等电子体
D.N2 与 CO 的化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关分子式为C8H10O的芳香化合物的推断正确的是( )
A.若C8H10O能与溴水发生取代反应,则1mol该有机物最多消耗2molBr2
B.若C8H10O遇FeCl3溶液不发生显色反应,则苯环上只能有一个取代基
C.若C8H10O能与NaOH溶液反应,则产物的化学式为C8H9ONa
D.若C8H10O能发生消去反应,则该有机物只有一种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在进行锌铜双液原电池实验时,若用铜丝代替盐桥(如图),外电路中仍然存在较小的电流,随着时间 的推移,电流逐渐减小。下列关于该装置说法错误的是
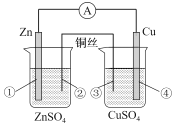
A.左池形成了原电池,Zn极的电势最高
B.铜丝②附近溶液的pH将升高
C.右池为电解池,铜丝③的反应式为 Cu-2eˉ=Cu2+
D.铜片④上有新的亮红色固体附着
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com