
| A. | Ag是短周期元素 | |
| B. | 主族元素的最高价都等于其最外层电子数 | |
| C. | Ne元素属于零族元素 | |
| D. | N的氢化物为H3N |
科目:高中化学 来源: 题型:解答题
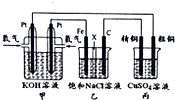 某同学设计了一个氢氧燃料电池(如图所示),目的是探究氯碱工业(人们习惯上把电解饱和食盐水的工业叫做氯碱工业)原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.
某同学设计了一个氢氧燃料电池(如图所示),目的是探究氯碱工业(人们习惯上把电解饱和食盐水的工业叫做氯碱工业)原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使酸性KMnO4褪色 | B. | 溴乙烷在NaOH乙醇溶液中加热 | ||
| C. | 乙醛的银镜反应 | D. | 溴乙烷在NaOH水溶液中加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中都含有离子键 | |
| B. | 离子化合物中的阳离子只能是金属离子 | |
| C. | 共价化合物也能含有离子键 | |
| D. | 离子化合物不能含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
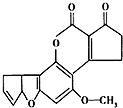 黄曲霉素AFTB1(如图)是污染粮食的真菌霉素.人类的特殊基因在黄曲霉素的作用下会发生突变,有转变成肝癌的可能性.与1mol黄曲霉素起反应的H2或NaOH的最大量分别是( )
黄曲霉素AFTB1(如图)是污染粮食的真菌霉素.人类的特殊基因在黄曲霉素的作用下会发生突变,有转变成肝癌的可能性.与1mol黄曲霉素起反应的H2或NaOH的最大量分别是( )| A. | 6mol,2mol | B. | 7mol,2mol | C. | 6mol,1mol | D. | 7mol,1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | N≡N | F-F | N-F |
| 键能:kJ/mol | 941.7 | 154.8 | 283.0 |
| A. | 过程F2(g)→2F(g)吸收能量 | |
| B. | 过程N(g)+3F(g)→NF3(g)放出能量 | |
| C. | 反应N2(g)+3F2(g)=2NF3(g)的△H<0 | |
| D. | NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com