
A和B在一定条件下可合成芳香族化合物E,G在标准状况下是气体,此情况下的密度为1.25g/L.各物质间相互转化关系如下所示:
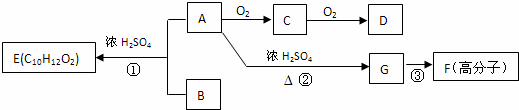
请回答下列问题:
(1)G中的官能团是 (用化学式表示),D中的官能团名称是 ,F的结构简式 .
(2)指出反应类型:① ,② ,③ .
(3)满足下列条件的B的同分异构体有 种.
①遇FeCl3溶液显紫色 ②能发生银镜反应 ③苯环上只有两个取代基
(4)写出化学方程式:A→C ;
C与新制的氢氧化铜悬浊液反应: .
考点: 有机物的推断.
专题: 有机物的化学性质及推断.
分析: G在标准状况下是气体,此情况下的密度为1.25g/L,其摩尔质量为1.25g/L×22.4L/mol=28g/mol,故G为CH2=CH2,乙烯发生加聚反应是高聚物F为 .A可以连续氧化生成D,则A为醇、C为醛、D为羧酸.A在浓硫酸、加热条件下生成G,则A为CH3CH2OH,C为CH3CHO,D为CH3COOH.A和B在一定条件下可合成芳香族化合物E,结合E的分子式与反应条件可知,B含有﹣COOH,故B的分子式为C10H12O2+H2O﹣CH3CH2OH=C8H8O2,B的不饱和度为
.A可以连续氧化生成D,则A为醇、C为醛、D为羧酸.A在浓硫酸、加热条件下生成G,则A为CH3CH2OH,C为CH3CHO,D为CH3COOH.A和B在一定条件下可合成芳香族化合物E,结合E的分子式与反应条件可知,B含有﹣COOH,故B的分子式为C10H12O2+H2O﹣CH3CH2OH=C8H8O2,B的不饱和度为 =5,故B为苯乙酸或甲基苯甲酸(有邻、间、对三种),据此解答.
=5,故B为苯乙酸或甲基苯甲酸(有邻、间、对三种),据此解答.
解答: 解:G在标准状况下是气体,此情况下的密度为1.25g/L,其摩尔质量为1.25g/L×22.4L/mol=28g/mol,故G为CH2=CH2,乙烯发生加聚反应是高聚物F为 .A可以连续氧化生成D,则A为醇、C为醛、D为羧酸.A在浓硫酸、加热条件下生成G,则A为CH3CH2OH,C为CH3CHO,D为CH3COOH.A和B在一定条件下可合成芳香族化合物E,结合E的分子式与反应条件可知,B含有﹣COOH,故B的分子式为C10H12O2+H2O﹣CH3CH2OH=C8H8O2,B的不饱和度为
.A可以连续氧化生成D,则A为醇、C为醛、D为羧酸.A在浓硫酸、加热条件下生成G,则A为CH3CH2OH,C为CH3CHO,D为CH3COOH.A和B在一定条件下可合成芳香族化合物E,结合E的分子式与反应条件可知,B含有﹣COOH,故B的分子式为C10H12O2+H2O﹣CH3CH2OH=C8H8O2,B的不饱和度为 =5,故B为苯乙酸或甲基苯甲酸(有邻、间、对三种),
=5,故B为苯乙酸或甲基苯甲酸(有邻、间、对三种),
(1)G为CH2=CH2,含有官能团是 ,D为CH3COOH,含有羧基,F的结构简式为
,D为CH3COOH,含有羧基,F的结构简式为 ,
,
故答案为: ;羧基;
;羧基; ;
;
(2)反应①属于酯化反应,反应②属于消去反应,反应③属于加聚反应,
故答案为:酯化反应;消去反应;加聚反应;
(3)满足下列条件B的同分异构体:①遇FeCl3溶液显紫色,含有酚羟基﹣OH,②能发生银镜反应,含有醛基﹣CHO,③苯环上只有两个取代基,取代基为﹣OH、﹣CH2CHO,有邻、间、对三种位置关系,故符合条件的B的同分异构体有3种,
故答案为:3;
(4)A→C的方程式为:2CH3CH2OH+O2 2CH3CHO+H2O,
2CH3CHO+H2O,
C与新制的氢氧化铜悬浊液反应为:CH3CHO+2Cu(OH)2 CH3COOH+Cu2 O↓+2H2O,
CH3COOH+Cu2 O↓+2H2O,
故答案为:2CH3CH2OH+O2 2CH3CHO+H2O;CH3CHO+2Cu(OH)2
2CH3CHO+H2O;CH3CHO+2Cu(OH)2 CH3COOH+Cu2 O↓+2H2O.
CH3COOH+Cu2 O↓+2H2O.
点评: 本题考查有机物的推断与合成,涉及醇、醛、羧酸、酯、酚、烯烃的性质等,难度中等,推断G为你乙烯是推断的关键,再结合A可以连续氧化进行推断,注意掌握官能团的性质与转化.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
运用元素周期律分析下面的推断,其中不正确的是( )
|
| A. | 锂(Li)与水反应比钠与水反应剧烈 |
|
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 |
|
| C. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 |
|
| D. | HBrO4的酸性比HIO4的酸性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
香叶醇是合成玫瑰香油的主要原料,其结构简式如下:下列有关香叶醇的叙述正确的是( )

|
| A. | 香叶醇的分子式为C10H18O |
|
| B. | 不能使溴的四氯化碳溶液褪色 |
|
| C. | 不能使酸性高锰酸钾溶液褪色 |
|
| D. | 能发生加成反应不能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
“三鹿奶粉”事件波及很广,据调查某些奶农为了提高鲜奶的“蛋白质”含量,往里面加了点三聚氰胺C3H6N6(见右图),三聚氰胺可由尿素合成.下列说法错误的是( )
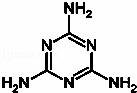
A. 尿素是人工合成的第一种有机物
B. 三聚氰胺不是芳香族化合物
C. 三聚氰胺属于氨基酸
D. 饮用含三聚氰胺的奶粉会导致肾结石
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述,正确的是(填序号) .
A、用NaOH溶液除去乙酸乙酯中混有的乙酸、乙醇,然后分液
B、分馏石油时,温度计的末端必须插入液面下
C、用分液漏斗分离环己烷和水的混合液体
D、用浓氨水洗涤做过银镜反应的试管
E、配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加到沉淀刚好溶解为止
F、蔗糖水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖.
查看答案和解析>>
科目:高中化学 来源: 题型:
有一澄清透明的溶液,只可能含有大量的Fe3+、Fe2+、H+、AlO2﹣、Al3+、CO32﹣、NO3﹣七种离子中的几种,向该溶液中逐滴加入一定量1mol/L NaOH溶液的过程中,开始没有沉淀,而后才有沉淀.则下列判断正确的是( )
A. 溶液中可能含有AlO2﹣
B. 溶液中可能含有NO3﹣
C. 溶液中一定不含Fe2+和Fe3+
D. 溶液中可能含有Fe3+,但一定不含Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中只可能有K+、Mg2+、AlO2﹣、SiO32﹣、CO32﹣、SO42﹣中的若干种离子.某同学对溶液进行了如图实验: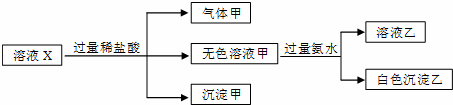
下列判断错误的是( )
A. 有气体甲生成,表明溶液X中一定含有CO32﹣
B. 沉淀甲不可能是硅酸镁
C. Al3+一定存在于溶液X中
D. 不可能确定SO42﹣是否存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
大气中硫、氮的氧化物是形成酸雨的主要物质.某地酸雨中可能含有下列离子:Na+、Ba2+、NH4+、Al3+、Cl﹣、SO32﹣、SO42﹣、NO3﹣等.某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成3份,进行如下实验:
试样 所加试剂 实验现象
第一份试液 滴加适量的淀粉KI溶液 呈蓝色
第二份试液 滴加用盐酸盐化的BaCl2溶液 有白色沉淀
第三份试液 滴加溶液,加热,加入的氢氧化钠溶液体积(V)与生成的沉淀、产生的气体关系(n)如右图. 
请回答下列问题:
(1)根据实验结果判断该酸雨中肯定不存在的离子是 .
写出试液中滴加淀粉KI溶液所发生反应的离子方程式: .
(3)设计实验方案,检验该试液中是否存在Cl﹣:
(4)该研究小组为了探究NO参与的硫酸型酸雨的形成,在烧瓶中充入含有少量NO的SO2气体,再慢慢通入O2,发生化学反应后,再喷洒适量蒸馏水即得硫酸型酸雨,则NO在上述反应中的作用是 .
(5)在0.5L密闭容器内加入NO2和SO2,为了测定在某种催化剂作用下反应:NO2(g)+SO2(g)⇌NO(g)+SO3(g)的反应速率,在t0C用气体传感器测得不同时间的NO2和SO2浓度如表(均不考虑温度变化对催化剂催化效率的影响):
时间/s 0 1 2 3 4 5
c(NO2)/mol•L﹣1 1.00×10﹣3 4.50×10﹣4 2.50×10﹣4 1.50×10﹣4 1.00×10﹣4 1.00×10﹣4
c(SO2)/mol•L﹣1 3.60×10﹣3 3.05×10﹣3 2.85×10﹣3 2.75×10﹣3 2.70×10﹣3 2.70×10﹣3
①前2s内NO的平均反应速率v(NO)= .
②t℃该反应的化学平衡常数K= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com