
分析 (1)氯酸钾具有氧化性能把浓盐酸氧化生成氯气;
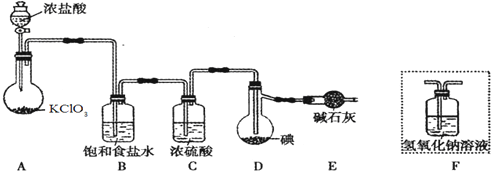
(2)制备的氯气中含有氯化氢,可以用饱和食盐水除去氯气中的氯化氢;装置F中的水蒸气进入装置D中,会使ICl水解;
(3)ICl与ICl3的沸点相差较大;
(4)①碘遇淀粉显蓝色;
②滴定过程中需要不断振荡,如果不振荡,则单质碘不能完全反应;
③实验2中比实验1多消耗的溶液体积为(V2-V1)ml,其物质的量的是0.001a(V2-V1)mol,
根据方程式②ICl+KI=I2+KCl和③I2+2Na2S2O3=2NaI+Na2S4O6可知:ICl~2Na2S2O3,求出ICl的物质的量,
再根据方程式①可知,5.00g该油脂样品所消耗的ICl的物质的量.
解答 解:(1)氯酸钾具有氧化性能把浓盐酸氧化生成氯气,则装置A中发生反应的化学方程式是KClO3+6HCl=KCl+3Cl2↑+3H2O;
故答案为:KClO3+6HCl=KCl+3Cl2↑+3H2O;
(2)浓盐酸易挥发生成的氯气中含有氯化氢,所以装置B中饱和食盐水的作用是除去氯气中的氯化氢,已知ICl易水解,若用装置F代替装置E,则装置F中的水蒸气会进入装置D中,使ICl水解,所以不能用装置F代替装置E;
故答案为:除去氯气中的氯化氢;装置F中的水蒸气会进入装置D中,使ICl水解;
(3)由于ICl与ICl3的沸点相差较大,因此若所制得的ICl中溶有少量ICl3杂质,提纯的方法是蒸馏,故答案为:C;
(4)①由于碘遇淀粉显蓝色,因此滴定过程中可用淀粉溶液作指示剂;故答案为:淀粉溶液;
②滴定过程中需要不断振荡,如果不振荡,则单质碘不能完全反应溶液就会褪色,从而导致消耗硫代硫酸钠的量减小,即会导致V1偏小;
故答案为:偏小;
③实验2中比实验1多消耗的溶液体积为(V2-V1)ml,则Na2S2O3的物质的量的是0.001a(V2-V1)mol,
根据方程式②ICl+KI=I2+KCl和③I2+2Na2S2O3=2NaI+Na2S4O6可知:ICl~2Na2S2O3,
所以ICl的物质的量是0.001a(V2-V1)mol×$\frac{1}{2}$,
由根据方程式①可知,5.00g该油脂样品所消耗的ICl的物质的量为0.001a(V2-V1)mol×$\frac{1}{2}$×$\frac{100ml}{10ml}$=5a(V2-V1)×10-3mol,故答案为:5a(V2-V1)×10-3.
点评 本题考查了物质制备实验方案设计,侧重于实验原理、基本操作、物质性质、数据处理等知识的考查,主要考查了学生的实验操作能力和数据处理能力,题目难度中等.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 项目 | 氨碱法 | 联合制碱法 |
| A. | 原料 | 食盐、氨气、生石灰 | 食盐、氨气、二氧化碳 |
| B. | 可能的副产物 | 氯化钙 | 氯化铵 |
| C. | 循环物质 | 氨气、二氧化碳 | 氨气、氯化钠 |
| D. | 评价 | 原料易得、产率高 | 设备简单、能耗低 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
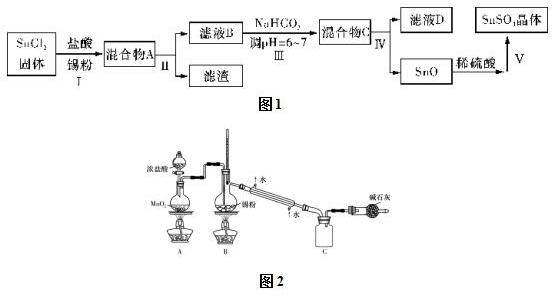
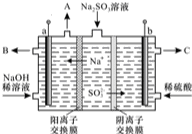 硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾.
硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
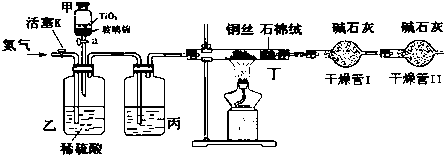
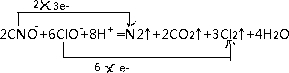 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
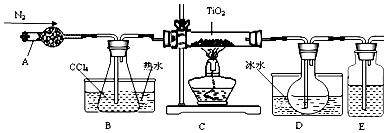
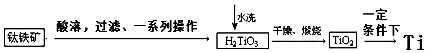
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
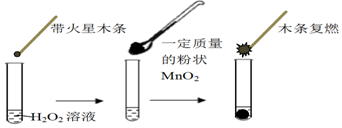
| MnO2的质量/g | 0.1 | 0.2 | 0.4 |
| 40s末O2体积/mL | 49 | 61 | 86 |
| 试管 | Ⅰ | Ⅱ | Ⅲ |
| 滴加试剂 | 5滴0.1mol•L-1FeCl3 | 5滴0.1mol•L-1 CuCl2 | 5滴0.3mol•L-1 NaCl |
| 产生气 泡情况 | 较快产生细小气泡 | 缓慢产生细小气泡 | 无气泡产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com