

| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的PH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的PH | 3.2 | 9.0 | 6.7 |
分析 氯化亚铁和氯化铜的混合液中,加入氧化剂可以将亚铁离子氧化为铁离子,调节pH可以将铁离子沉淀,得到氯化铜的水溶液,然后再酸性环境下蒸发浓缩、冷却结晶,过滤、洗涤、干燥即可得到氯化铜晶体.
(1)加入氧化剂,将Fe2+氧化为Fe3+,易除去,选择的氧化剂不能引进新的杂质离子是最佳氧化剂;
(2)中和溶液的酸性,调节pH,将铁离子沉淀,铜离子不沉淀,可以加入CuO或Cu(OH)2、CuCO3、Cu2(OH)2CO3;
(3)从溶液中获得晶体要经过蒸发浓缩、冷却结晶、过滤三步操作;
(4)KMnO4溶液具有强氧化性,能腐蚀碱式滴定管的胶管;Fe2+与MnO4-反应,Mn元素的化合价由+7价降低为+2价,Fe元素的化合价由+2价升高为+3价,由电子守恒、电荷守恒、原子守恒解答.
解答 解:(1)根据实验目的,加入氧化剂的目的是将Fe2+氧化成Fe3+,便于生成Fe(OH)3沉淀而与Cu2+分离,K2Cr2O7、NaClO、H2O2、KMnO4都具有氧化性,能将亚铁离子氧化,但是K2Cr2O7、NaClO、KMnO4能引进新的杂质离子,双氧水是绿色氧化剂,得到的还原产物是水,不会引进杂质离子,
故答案为:C;
(2)加入的物质Y可调节,使Fe3+全部沉淀,同时不引进新杂质,铁离子在水中存在水解平衡:Fe3++3H2O?Fe(OH)3+3H+,用Cu(OH)2、CuCO3、CuO、Cu2(OH)2CO3等,
中和溶液的酸性,能促进水解平衡向正反应方向移动,调节pH,可以将铁离子沉淀(Fe3+氢氧化物完全沉淀时的PH:3.2),同时引入铜离子,无新的金属离子引入,且铜离子不沉淀(Cu2+氢氧化物开始沉淀时的PH:4.7),氢氧化钠和氨气都能使铜离子沉淀,无法分离Fe3+、Cu2+,
故答案为:AC;
(3)结晶水合物,为防止结晶水散失,从溶液中获得晶体通常采用降温结晶,所以从溶液中获得氯化铜晶体(CuCl2•2H20)要经过蒸发浓缩、冷却结晶、过滤三步操作,
故答案为:蒸发浓缩;冷却结晶;
(4)KMnO4溶液具有强氧化性,能腐蚀碱式滴定管的胶管,所以选择酸式滴定管,测定溶液Ⅰ中Fe2+的浓度,用KMnO4标准溶液滴定,Fe2+与MnO4-反应,Mn元素的化合价由+7价降低为+2价,Fe元素的化合价由+2价升高为+3价,由电子守恒、电荷守恒、原子守恒可知,离子反应为MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O,
故答案为:酸式;MnO4-+8H++5Fe2+=Mn2++5Fe3++4H2O.
点评 本题是一道物质的分离和提纯的实验方案设计题,题目考查的知识点较多,涉及氧化还原反应原理的应用、调节pH除杂质、盐的水解原理的应用等,考查学生分析解决问题以及灵活应用所学知识的能力,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.使石蕊试液变红的溶液中:I-、MnO 、NO
、NO 、Na+
、Na+
B.含有大量Fe3+的溶液:NH 、HCO
、HCO 、SO
、SO 、AlO
、AlO
C.水电离出c(H+)=1.0×10-12mol/L的溶液:Cl-、Na+、ClO-、NH
D. 澄清透明的溶液:Cu2+、Fe3+、SO
澄清透明的溶液:Cu2+、Fe3+、SO 、NO
、NO
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
| 溶解度(25℃,g/100g水) | 0.3 | 遇热水水解 | 0.04 | 互溶 |
| 沸点(℃) | 179.6 | 138.6 | 300 | 118 |
| 相对分子质量 | 106 | 102 | 148 | 60 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: +H2O+H2SO4$\stackrel{100-130℃}{→}$
+H2O+H2SO4$\stackrel{100-130℃}{→}$ +NH4HSO4
+NH4HSO4 +Cu(OH)2→
+Cu(OH)2→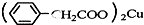 +H2O
+H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 草酸是一种重要的化工原料,常用于有机合成,它属于二元弱酸,易溶于乙醇、水、微溶于乙醚.以甘蔗碎渣(主要成分为纤维素)为原料制取草酸的工艺流程如下:
草酸是一种重要的化工原料,常用于有机合成,它属于二元弱酸,易溶于乙醇、水、微溶于乙醚.以甘蔗碎渣(主要成分为纤维素)为原料制取草酸的工艺流程如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O与18O互为同位素,H218O与D218O互为同素异形体,甲醇、乙二醇与丙三醇互为同系物 | |
| B. | 在SiO2晶体中,一个Si原子和2个O原子形成两个共价键 | |
| C. | 1L0.5mol/L 稀硫酸与1L 1mol/L 氢氧化钠溶液反应放出57.3kJ的热:H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(1);△H=-114.6 kJ/mol | |
| D. | 碳酸钠水溶液显碱性的原因:CO32-+2H2O?H2CO3+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | KCl溶液(CaCl2) | 加K2CO3溶液,过滤,再加适量盐酸 |
| B | NaNO3溶液(AgNO3) | 加适量NaCl溶液,过滤 |
| C | NaCl溶液(I2) | 加酒精,分液 |
| D | KBr溶液(Br2) | 加CCl4,分液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com