
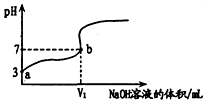
 常温下,用0.1000mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程溶液pH随NaOH溶液的体积的变化曲线如图所示(忽略中和热效应).下列说法不正确的是( )
常温下,用0.1000mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程溶液pH随NaOH溶液的体积的变化曲线如图所示(忽略中和热效应).下列说法不正确的是( )| A. | 常温下,HA的电离常数K(HA)约为10-5 | |
| B. | v1<20 | |
| C. | 溶液中水的电离程度:a点>b点 | |
| D. | 滴定过程为了确定滴定终点,最合适的指示剂是酚酞 |
分析 0.1000mol/LHA溶液的pH=3,说明HA为弱酸,在溶液中只能部分电离出氢离子,
A.0.1000mol/LHA溶液的pH=3,其溶液中氢离子浓度为0.001mol/L,c(A-)≈c(H+)、c(HA)≈0.1000mol/L,据此结合电离平衡常数的表达式计算HA的电离常数K(HA);
B.v1=20时二者恰好反应生成强碱弱酸盐NaA,溶液呈碱性,若为中性,则加入的氢氧化钠溶液体积稍小;
C.a点溶液呈酸性,抑制了水的电离,b点溶液为中性,基本不影响水的电离;
D.二者恰好反应生成强碱弱酸盐NaA,溶液呈碱性,结合酚酞的变色范围分析.
解答 解:0.1000mol/LHA溶液的pH=3,说明HA为弱酸,在溶液中只能部分电离出氢离子,
A.0.1000mol/LHA溶液的pH=3,其溶液中氢离子浓度为0.001mol/L,c(A-)≈c(H+)、c(HA)≈0.1000mol/L,常温下HA的电离常数K(HA)=$\frac{1×1{0}^{-3}×1×1{0}^{-3}}{0.1000}$=10-5,故A正确;
B.v1时溶液的pH=7,溶液呈中性,而v1=20时二者恰好反应生成强碱弱酸盐NaA,溶液呈碱性,若使反应后溶液呈中性,则加入的氢氧化钠溶液体积偏小,即v1<20,故B正确;
C.根据图象可知,a点为0.1000mol/LHA溶液,氢离子抑制了水的电离,而b点溶液为中性,不影响水的电离,则溶液中水的电离程度:a点<b点,故C错误;
D.等浓度、等体积的两溶液恰好反应生成强碱弱酸盐NaA,溶液呈碱性,酚酞的变色范围为8~10,所以滴定过程为了确定滴定终点,最合适的指示剂是酚酞,故D正确;
故选C.
点评 本题考查溶液酸碱性与溶液pH的关系就计算,题目难度中等,明确图象曲线各点表示含义为解答关键,注意掌握溶液酸碱性与溶液pH的关系,试题培养了学生的分析能力及化学计算能力.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
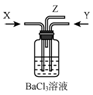 浓硫酸共热产生的气体X和铜和浓硝酸反应产生的气体Y间时通入盛有足量氯化钡溶液的气瓶中(如图装置),下列有关说法不正确的是( )
浓硫酸共热产生的气体X和铜和浓硝酸反应产生的气体Y间时通入盛有足量氯化钡溶液的气瓶中(如图装置),下列有关说法不正确的是( )| A. | 洗气瓶中产生的沉淀是碳酸钡 | B. | 洗气瓶中产生的沉淀是亚硫酸钡 | ||
| C. | 洗气瓶中有氧化还原反应发生 | D. | 在Z导管口有红棕色气体出现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤⑦ | B. | ⑤②①③⑥ | C. | ⑤②①④⑦ | D. | ①②⑤③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 烷烃的同系物可用通式CnH2n+2表示 | |
| B. | 同系物的化学性质相似 | |
| C. | 同系物的物理性质相同 | |
| D. | 同分异构体的化学性质一定不相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | ① | ② | ③ | ④ |
| 科学家 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
| 工作 | 发现“八音律”,指出从某一指定的元素起,第八个元素是第一个元素的某种重复 | 创立 近代原子论,率先开始相对原子质量的测定工作 | 发现了5组性质相似的“三元素组”,中间元素的相对原子质量为前后两种元素相对原子质量的算术平均值 | 认为 各元素组之间并非毫不相关,可以用相对原子质量把它们按从小到大的顺序串联 |
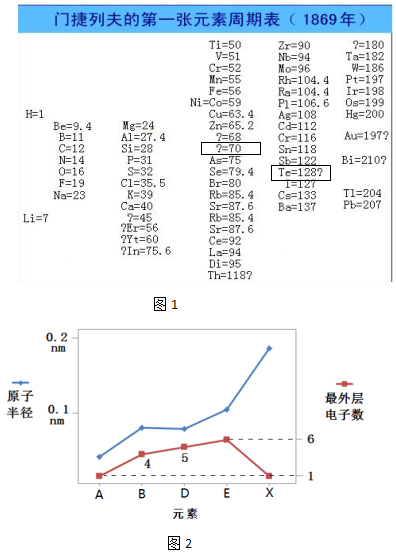
 ,写出Z元素气态氢化物的电子式:
,写出Z元素气态氢化物的电子式: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的液态单质可在医疗上用于冷冻麻醉 | |
| B. | Y、M两元素气态氢化物的稳定性:Y<M | |
| C. | 工业上制备Z的单质可电解其熔融态的氧化物 | |
| D. | 氧化物XO2与MO2均具有漂白性,且漂白原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲为C,X为O2 | B. | 甲为SO2,X为NaOH溶液 | ||
| C. | 甲为Fe,X为Cl2 | D. | 甲为硝酸溶液,X为Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com