
【题目】某研究小组按下列路线合成药物奥沙拉秦:
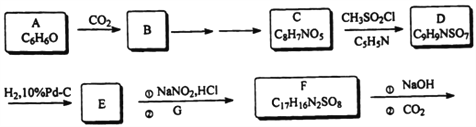
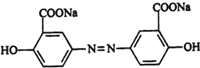 奥沙拉秦
奥沙拉秦
己知:(1)物质G是由物质B转化为物质C的一种中间产物
(2)R-NO2 ![]() R-NH2
R-NH2
(3)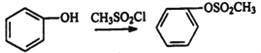
请回答:
(1)化合物A的结构简式_________________________。
(2)下列说法正确的是___________。
A.化合物A→B的反应是取代反应
B.化合物E既可以与HCl,可以与NaOH溶液反应
C.化合物F遇到FeCl3能发生显色反应
D.奥沙拉秦的分子式是C14H8N2O6Na2
(3)设计由化合物B生成化合物C的合成路线(用流程图表示,试剂任选)______________。
(4)写出C→D的化学方程式_____________________________________。
(5)化合物C可能的同分异构体的结构简式________________,须同时符合:
①1H-NMR谱表明分子中有3 种氢原子;
②IR谱显示含有苯环,N原子不与苯环直接相连接,乙酰基(CH3CO-);
③遇到FeCl3显色。
【答案】 ![]() BCD
BCD 

![]() 、
、 、
、 、
、
【解析】根据A的化学式可知,A为苯酚(![]() ),根据已知条件(2)可知,D中的硝基被还原生成氨基,因此E的化学式为C9H11NSO5,根据已知条件(3)可知,C中的酚羟基中的氢原子被CH3SO2-取代,因此C中含有硝基、酚羟基根据A与C的化学式的区别,A与二氧化碳发生加成反应生成了羧基,结合奥沙拉秦(
),根据已知条件(2)可知,D中的硝基被还原生成氨基,因此E的化学式为C9H11NSO5,根据已知条件(3)可知,C中的酚羟基中的氢原子被CH3SO2-取代,因此C中含有硝基、酚羟基根据A与C的化学式的区别,A与二氧化碳发生加成反应生成了羧基,结合奥沙拉秦( )的结构可知,B为
)的结构可知,B为 ;根据C 的化学式,C为
;根据C 的化学式,C为 ,则D为
,则D为 ,E为
,E为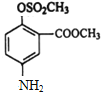 ,F为
,F为 。
。
(1)根据上述分析,化合物A为![]() ,故答案为:
,故答案为:![]() ;
;
(2)A.根据上述分析,化合物A→B的反应是加成反应,故A错误;B.化合物E( )中含有氨基,可以与HCl反应,含有酯基可以与NaOH溶液反应,故B正确;C.化合物F(
)中含有氨基,可以与HCl反应,含有酯基可以与NaOH溶液反应,故B正确;C.化合物F( )中含有酚羟基,遇到FeCl3能发生显色反应,故C正确;D.根据奥沙拉秦的结构简式(
)中含有酚羟基,遇到FeCl3能发生显色反应,故C正确;D.根据奥沙拉秦的结构简式( )可知的分子式是C14H8N2O6Na2,故D正确;故选BCD;
)可知的分子式是C14H8N2O6Na2,故D正确;故选BCD;
(3)由化合物B生成化合物C,可以有B首先与甲醇反应生成酯基,然后进行苯环上的硝化反应,故答案为: ;
;
(4)根据已知条件(3)可知,C中的酚羟基中的氢原子被CH3SO2-取代生成D,反应的化学方程式为 ,故答案为:
,故答案为: ;
;
(5)化合物C为 。①1H-NMR谱表明分子中有3 种氢原子;
。①1H-NMR谱表明分子中有3 种氢原子;
②IR谱显示含有苯环,N原子不与苯环直接相连接,乙酰基(CH3CO-);
③遇到FeCl3显色,说明含有酚羟基,满足条件的同分异构体有:![]() 、
、 、
、 、
、 ,故答案为:
,故答案为:![]() 、
、 、
、 、
、 。
。


 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】下列有关人类重要的营养物质的说法中,正确的是
A. 油脂属于酯类物质,是一种高分子化合物
B. 淀粉和纤维素及蔗糖等均属于糖类物质
C. 植物体内主要含纤维素,所以植物的生命现象和蛋白质无关
D. 淀粉纤维素油脂和蛋白质是人类的主食,它们均能在人的胃中被分解和消化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图甲是一种利用微生物将废水中的尿素(H2NCONH2)直接转化为对环境友好物质的原电池装置。现利用甲装置产生的电能对乙装置中的饱和食盐水进行电解(A、B皆为石墨电极)。下列说法中不正确的是( )

①M电极反应式:H2NCONH2+H2O+6e-=CO2↑+N2↑+6H+
②当A电极产生11.2mL气体(标况)时,则N电极消耗25×10-4mol气体
③甲中H+透过质子交换膜由右向左移动
④A电极应与X相连接
⑤反应一段时间后,乙装置U型管中的溶液pH变大
A. ①③ B. ①③⑤ C. ①②③ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4·yH2O),做如下实验:将固体加热,测量剩余固体的质量随时间的变化关系,如图所示。
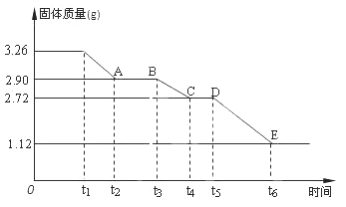
(1)t5~ t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色的气体物质的量是_______________________;
(2)x∶y=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明代宋应星著的《天工开物》中有关于“火法”冶炼锌的工艺记载:“炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。”下列说法不正确的是(注:炉甘石的主要成分为碳酸锌)
A. 该冶炼锌的反应属于置换反应
B. 煤炭中起作用的主要成分是C
C. 冶炼Zn的反应方程式为:ZnCO3+2C![]() Zn+3CO↑
Zn+3CO↑
D. 倭铅是指金属锌和铅的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 氧化还原反应一定属于四大基本反应类型
B. 氧化还原反应中,反应物不是氧化剂就是还原剂
C. 在氧化还原反应中,氧化剂和还原剂既可以是不同物质也可以是同种物质
D. 失电子越多,还原性越强,得电子越多,氧化性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.2L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,对于该溶液成分。下列说法不正确的是( )

A. NaCl的物质的量为0.2mol
B. 溶质MgCl2的质量为9g
C. 该混合液中BaCl2的物质的量为0.1mol
D. 将该混合液加水稀释至体积为1L,稀释后溶液中Ba2+的物质的量浓度为0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以酸性氢氧燃料电池为电源进行电解的实验装置如图所示。下列说法正确的是( )
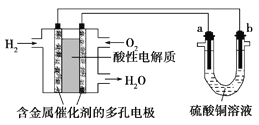
A. 燃料电池工作时,正极反应为O2+2H2O+4e-===4OH-
B. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
C. 电解过程中SO42— 移向b极
D. a、b两极若是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com