
下列实验方案合理的是( )。
A.用通入酸性高锰酸钾溶液的方法除去乙烯中混有的二氧化硫
B.用加入浓溴水的方法分离苯和苯酚的混合物
C.用灼热的铜丝网除去N2中混有的少量O2
D.用燃烧的方法除去CO2中混有的少量CO
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
已知下述三个实验均能发生化学反应。
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铁钉放入氯化铁溶液中 |
下列判断正确的是 ( )。
A.实验①和③中的铁钉只作还原剂
B.上述实验证明氧化性:Fe3+>Fe2+>Cu2+
C.实验②中Fe2+既显氧化性又显还原性
D.实验③中反应的离子方程式为Fe+Fe3+===2Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
1判断正误,正确的划“√”,错误的划“×”
(1)CH3COOH溶液加水稀释后,溶液中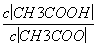 的值减小( )
的值减小( )
(2013·江苏,11C)
(2)室温下,对于0.10 mol·L-1的氨水,加水稀释后,溶液中c(NH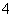 )·c(OH-)变大( )
)·c(OH-)变大( )
(2013·福建理综,8B)
(3)25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH( )
(2013·重庆理综,2B)
(4)稀醋酸加水稀释,醋酸的电离程度增大,溶液的pH减小( )
(2012·重庆理综,10B)
(5)中和等体积、等物质的量浓度的盐酸和醋酸所消耗的n(NaOH)相等( )
(2012·福建理综,10C)
查看答案和解析>>
科目:高中化学 来源: 题型:
为了证明一水合氨(NH3·H2O)是弱电解质,甲、乙、丙三人分别选用下列试剂进行实验:0.010 mol·L-1氨水、0.1 mol·L-1 NH4Cl溶液、NH4Cl晶体、酚酞溶液、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定一水合氨是弱电解质,你认为这一方法是否正确?________(填“正确”或“不正确”),并说明理由:
________________________________________________________________________。
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测其pH=b,若要确认NH3·H2O是弱电解质,则a、b值应满足什么关系?______________(用等式或不等式表示)。
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞溶液,显粉红色,再加入少量NH4Cl晶体,颜色变________(填“深”或“浅”)。你认为这一方法能否证明NH3·H2O是弱电解质?________(填“能”或“否”),并说明原因:
________________________________________________________________________。
(4)请你根据所提供的试剂,再提出一个合理又简便的方案证明NH3·H2O是弱电解质:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下有关元素性质的说法不正确的是 ( )。
A.具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4 原子半径最大的是①
B.具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4第一电离能最大的是③
C.①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数增大而递增的是④
D.某元素气态基态原子的逐级电离能(kJ·mol-1)分别为738、1 451、7 733、10 540、13 630、17 995、21 703,当它与氯气反应时可能生成的阳离子是X3+
查看答案和解析>>
科目:高中化学 来源: 题型:
用铁制备较纯净的三氧化二铁,下列实验方案最好的是( )
A.使铁在潮湿的空气中缓慢氧化
B.铁在氯气中燃烧,加水溶解,加入足量NaOH溶液,过滤、洗涤、然后充分加热分解
C.使铁溶解于稀硫酸,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
D.使铁与足量稀硝酸反应,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
查看答案和解析>>
科目:高中化学 来源: 题型:
有关溶液中所含离子的检验,下列判断中正确的是( )
A.加入硝酸酸化,再滴加KSCN溶液后有红色物质生成,则原溶液中一定有Fe3+存在
B.加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO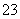 存在
存在
C.用某溶液做焰色反应实验时火焰为黄色,则该溶液中一定有钠元素,可能有钾元素
D.分别含有Mg2+、Cu2+、Fe2+和Na+的四种盐酸盐溶液,只用NaOH溶液是不能一次鉴别开的
查看答案和解析>>
科目:高中化学 来源: 题型:
图中A~J均为有机化合物,根据图中的信息,回答下列问题。
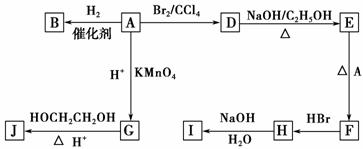
(1)环状化合物A的相对分子质量为82,其中含碳87.80%,含氢12.2%。B的一氯代物仅有一种,B的结构简式为_________________________。
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,则M的结构简式为__________________________________。
(3)由A生成D的反应类型是________,由D生成E的反应类型是________。
(4)G的分子式为C6H10O4,0.146 g G需用20 mL 0.100 mol·L-1 NaOH溶液完全中和,J是一种高分子化合物,则由G转化为J的化学方程式为________________________________________________________________
________________________________________________________________________;
(5)分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生如下反应:
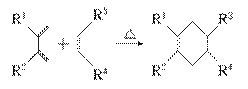
则由E和A反应生成F的化学方程式为__________________________________________________________________
________________________________________________________________________。
(6)H中含有的官能团是________,I中含有的官能团是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在铜的冶炼过程中有如下反应发生
5FeS2+14CuSO4+12H2O===7Cu2S+5FeSO4+12H2SO4
关于此反应,下列说法正确的是( )
A.Cu2S既是氧化产物,又是还原产物
B.5 mol FeS2发生反应,有10 mol电子转移
C.FeS2只作还原剂
D.产物中的SO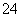 有一部分是氧化产物
有一部分是氧化产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com