
CO(g)与H2O(g)反应过程的能量变化如下图所示,有关两者反应说法正确的是( )

A.该反应为吸热反应
B.CO(g)和H2O(g)所具有的总能量大于CO2(g)和H2(g)具有的总能量
C.反应的热化学方程式:CO(g)+H2O(g)===CO2(g)+H2(g);ΔH=+41kJ·mol-1
D.1mol CO2(g)和1mol H2(g)反应生成1mol CO(g)和H2O(g)要放出41kJ的热量
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:福建省莆田一中2010-2011学年高一下学期第一学段考试化学试题 题型:013
|
反应:CO(g)+H2O(g)=CO2(g)+H2(g)的能量变化如图所示,有关该反应的说法正确的是
| |
| [ ] | |
A. |
该反应为吸热反应 |
B. |
1 mol CO2(g)和1 mol H2(g)反应生成1 mol CO(g)和1 mol H2O(g)要放出41 kJ热量 |
C. |
反应的热化学方程式是:CO(g)+H2O(g)=CO2(g)+H2(g)ΔH=+41 kJ/mol |
D. |
CO(g)与H2O(g)所具有的总能量大于CO2(g)与H2(g)所具有的总能量 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年云南省大理州宾川县第四高级中学高二4月月考化学卷(带解析) 题型:单选题
CO(g)与H2O(g)反应过程的能量变化如下图所示,有关两者反应说法正确的是( )
| A.该反应为吸热反应 |
| B.CO(g)和H2O(g)所具有的总能量大于CO2(g)和H2(g)具有的总能量 |
| C.反应的热化学方程式:CO(g)+H2O(g)===CO2(g)+H2(g);ΔH=+41kJ·mol-1 |
| D.1mol CO2(g)和1mol H2(g)反应生成1mol CO(g)和H2O(g)要放出41kJ的热量 |
查看答案和解析>>
科目:高中化学 来源:2015届江苏省徐州市高二上学期期末考试化学试卷(选修)(解析版) 题型:填空题
化学反应中既有物质变化,又有能量变化,释放或吸收热量是化学反应中能量变化的主要形式之一。已知C(石墨)、H2(g)燃烧的热化学方程式分别为:
① C(石墨)+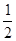 O2(g)=CO(g)
O2(g)=CO(g) 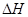 =-111.0 KJ·mol-1
=-111.0 KJ·mol-1
② H2(g)+
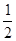 O2(g) =H20(g)
O2(g) =H20(g) 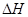 =-242.0 kJ·mol-1
=-242.0 kJ·mol-1
③ C(石墨)+O2(g)=CO2(g)
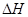 =-394.0 kJ·mol-1
=-394.0 kJ·mol-1
请解答下列问题:
(1)化学反应中有能量变化的本质原因是反应过程中有 的断裂和形成。上述三个反应都是 (填“吸热”或“放热”)反应。
(2)在热化学方程式中,需要标明反应物及生成物的状态的原因是 ;在①中,02的化学计量数“1/2”是表示 (填字母)。
a.分子个数 b.物质的量 c.气体的体积
(3)反应2H20(g)=2H2(g)+02(g)的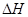 = KJ·mol-1。
= KJ·mol-1。
(4)若C(金刚石)+02(g)=C02(g)的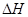 =-395.0 kJ·mol-1,则稳定性:金刚石 (填“>”、“<”或“=”)石墨。
=-395.0 kJ·mol-1,则稳定性:金刚石 (填“>”、“<”或“=”)石墨。
(5)已知形成H20(g)中的2 mol H-O键能放出926.0 kJ的能量,形成1 mol 02(g)中的共价键能放出498.0 kJ的能量,则断裂1 mol H2(g)中的H-H键需要的能量 KJ。
(6)工业制氢气的一个重要途径是用CO(g)与H2O(g)反应生成C02(g)和H2(g),则该反应的热化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应中既有物质变化,又有能量变化,释放或吸收热量是化学反应中能量变化的主要形式之一。已知C(石墨)、H2(g)燃烧的热化学方程式分别为:
① C(石墨)+![]() O2(g)=CO(g)
O2(g)=CO(g) ![]() =-111.0 KJ·mol-1
=-111.0 KJ·mol-1
② H2(g)+ ![]() 02(g) =H20(g)
02(g) =H20(g) ![]() =-242.0 kJ·mol-1
=-242.0 kJ·mol-1
③ C(石墨)+02(g)=CO2(g) ![]() =-394.0 kJ·mol-1
=-394.0 kJ·mol-1
请解答下列问题:
(1)化学反应中有能量变化的本质原因是反应过程中有 的断裂和形成。上述三个反应都是 (填“吸热”或“放热”)反应。
(2)在热化学方程式中,需要标明反应物及生成物的状态的原因是
;在①中,02的化学计量数“1/2”是表示 (填字母)。
a.分子个数 b.物质的量 c.气体的体积
(3)反应2H20(g)=2H2(g)+02(g)的![]() = KJ·mol-1。
= KJ·mol-1。
(4)若C(金刚石)+02(g)=C02(g)的![]() =-395.0 kJ·mol-1,则稳定性:金刚石
=-395.0 kJ·mol-1,则稳定性:金刚石
(填“>”、“<”或“=”)石墨。
(5)已知形成H20(g)中的2 mol H-O键能放出926.0 kJ的能量,形成1 mol 02(g)中的共价键能放出498.0 kJ的能量,则断裂1 mol H2(g)中的H-H键需要的能量 KJ。
(6)工业制氢气的一个重要途径是用CO(g)与H2O(g)反应生成C02(g)和H2(g),则该反应的热化学方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com