
【题目】某同学用下列装置制备并检验Cl2的性质,相关说法正确的是
A.  如果MnO2过量,浓盐酸就可全部被消耗
如果MnO2过量,浓盐酸就可全部被消耗
B.  量筒中发生了取代反应
量筒中发生了取代反应
C. 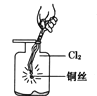 生成蓝色的烟
生成蓝色的烟
D.  湿润的有色布条褪色说明了Cl2具有漂白性
湿润的有色布条褪色说明了Cl2具有漂白性
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,反应A2(g)+B2(g)![]() 2AB(g)达到平衡的标志是
2AB(g)达到平衡的标志是
A. 单位时间内生成n mol A2的同时生成n mol AB
B. 容器内的总压强不随时间的变化而变化
C. 单位时间内生成2n mol AB的同时生成n mol B2
D. 单位时间内生成n mol A2的同时生成n mol B2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t ℃,体积固定的密闭容器中,发生反应A(g)+3B(g)![]() 2C(g),开始充入1 mol A和3 mol B,达平衡后再充入2 mol C,则平衡
2C(g),开始充入1 mol A和3 mol B,达平衡后再充入2 mol C,则平衡
A. 正向移动 B. 逆向移动
C. 不移动 D. 再次达新平衡时,C的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
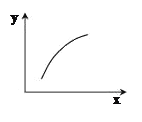
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇的官能团名称是______,结构简式为______;羧酸的官能团名称是______,结构简式为_______。二者在一定条件下发生反应的类型是______,写出乙酸和乙醇反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中,保持一定温度,在一定条件下进行如下反应A(g)+2B(g)![]() 3C(g),已知起始时加入2 mol A(g)和3 mol B(g),达平衡后,生成a mol C(g)。此时,C(g)在反应混合气体中的体积分数为_____________(用含字母a的代数式表示)。
3C(g),已知起始时加入2 mol A(g)和3 mol B(g),达平衡后,生成a mol C(g)。此时,C(g)在反应混合气体中的体积分数为_____________(用含字母a的代数式表示)。
(1)相同实验条件下,若在同一容器中改为开始加入1 mol A和1.5mol B,达平衡时C的物质的量为________mol(用含字母a的代数式表示)。此时C在反应混合物中的体积分数_____________(填“增大”、“减小”或“不变”)。
(2)相同实验条件下,若在同一容器中改为开始时加入2 mol A和2 mol B,达平衡时,要求C在混合物中体积分数与(1)相同,则开始时还需加入_________mol C,平衡时C的物质的量为_______________mol(用含字母a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N2O4反应能放出大量的热。
(1)25 ℃,1.00 g N2H4 (l)与足量N2O4 (l)完全反应生成N2 (g)和H2O (l),放出19.14 kJ的热量。则反应2N2H4 (l)+N2O4 (l)=3N2 (g)+4H2O (l)的△H= __________ kJ/mol。
(2)已知:2NO2(g)![]() N2O4(g) △H=-57.20 kJ/mol。一定温度下,在密闭容器中反应2NO2(g)
N2O4(g) △H=-57.20 kJ/mol。一定温度下,在密闭容器中反应2NO2(g)![]() N2O4(g)达到平衡。
N2O4(g)达到平衡。
①其他条件不变时,下列措施能提高NO2转化率的是 ________。
A.升高温度 B.降低温度 C.增加NO2的浓度 D.扩大容器体积
②平衡时,c(NO2)=0.0300 mol/L、c(N2O4)=0.0120 mol/L。若升高温度,则平衡常数____________(填“增大”、“减小”或“不变”);若起始NO2和N2O4的浓度均为0.0100 mol/L,则v(正)______v(逆)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化符合图示的是( )
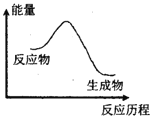
①KMnO4分解制O2 ②铝与盐酸的反应
③钠与水反应 ④二氧化碳与灼热的木炭反应
⑤Ba(OH)2·8H2O和NH4Cl的反应.⑥硫酸与氢氧化钾的反应
A. ②④⑥B. ②③⑤C. ②③⑥D. ③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)FeSO4可转化为FeCO3,FeCO3在空气中加热可制得铁系氧化物材料。已知25℃,101kPa时:4Fe(s)+3O2(g)
=2Fe2O3(s)ΔH=-1648kJ/mol,C(s)+O2(g)=CO2(g) ΔH=-393kJ/mol,2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480kJ/mol,FeCO3在空气中加热反应生成Fe2O3的热化学方程式为_______。
(2)一定条件下,向容积可变的密闭容器中通入N2和H2,发生反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0达到平衡后,试回答下列问题:
2NH3(g) ΔH<0达到平衡后,试回答下列问题:
①达到平衡后,若其它条件不变,把容器体积缩小一半,平衡将____(填“向逆反应方向”、“向正反应方向”或“不”)移动,平衡常数K将_____ (填“增大”、“减小”或“不变”)。
②达到平衡后,在恒压条件下,向容器中通人氦气(He),氮气的转化率将___(填“增大”、“减小”或“不变”)。
(3)AlCl3溶液加热蒸干并灼烧最终得到物质是________(填化学式),将NaHCO3与Al2(SO4)3溶液混合后可做泡沫灭火剂,其原理是_______(用离子方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com