
 、ClO-
、ClO- 、OH-
、OH- 、HCO3-
、HCO3-
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
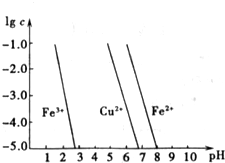 铁、铜都是人类最早使用的金属,它们的单质及化合物应用非常广泛.
铁、铜都是人类最早使用的金属,它们的单质及化合物应用非常广泛.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
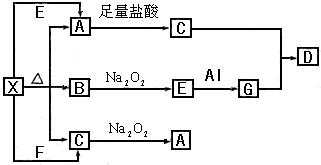 下图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A.无色液体B.无色气体C各1mol.X.E.G的焰色反应均为黄色.
下图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A.无色液体B.无色气体C各1mol.X.E.G的焰色反应均为黄色.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
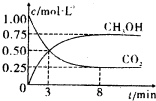 碳和碳的化合物在人类生产、生活中的应用非常广泛,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
碳和碳的化合物在人类生产、生活中的应用非常广泛,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.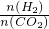 =a,则a的取值范围为______.
=a,则a的取值范围为______.查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
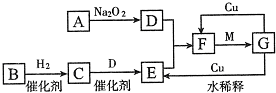 如图表示由短周期元素组成的一些物质之间的转化关系(某些反应产物已略去).各方框表示有关的一种反应物或生成物(某些物质已经略去),其中A、B、D在常温下均为无色无刺激性气味的气体,C是使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体.
如图表示由短周期元素组成的一些物质之间的转化关系(某些反应产物已略去).各方框表示有关的一种反应物或生成物(某些物质已经略去),其中A、B、D在常温下均为无色无刺激性气味的气体,C是使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com