
| A. | 250 mL 1 mol•L-1FeCl3溶液中,阴、阳离子总数为NA | |
| B. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 0.1mol HCN分子中含有的π键数目为0.2NA |
分析 A.三价铁离子在水溶液中会水解;
B.氢氧化钠溶液中,氢氧根离子抑制了水的电离,溶液中的氢离子是水电离的,则水电离的氢氧根离子浓度=氢离子浓度=1×10-13mol/L;
C.1个氧气分子得到4个电子生成二价氧;
D.HCN的结构式为H-C≡N.
解答 解:A.1 mol铁离子会水解,生成3mol的氢离子,所以250mL1mol•L-1FeCl3溶液中,阴、阳离子总数大于阿伏加德罗常数,故A错误;
B.在氢氧化钠溶液中,水的电离被抑制,溶液中的氢离子全部来自于水的电离,而在pH=13的氢氧化钠溶液中,氢离子浓度为10-13mol/L,故此溶液中水电离出的氢离子的物质的量为10-13mol,而水电离出的氢氧根的个数等于其电离出的氢离子的个数,故此溶液中水电离出的氢氧根的个数为10-13NA,故B错误;
C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA,故C错误;
D.HCN的结构式为H-C≡N,故1molHCN中含2molπ键,故0.1molHCN中含0.2NA条π键,故D正确;
故选D.
点评 本题考查了盐类水解、水的电离及其影响、原电池原理、分子结构等,题目难度中等,明确酸碱溶液抑制了水的电离,能够水解的盐促进了水的电离为解答关键,试题培养了学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | pH:②>③>④>① | B. | c(CH3COO-):②>④>③>① | ||
| C. | 溶液中c(H+):①>③>②>④ | D. | c(CH3COOH):①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与氢气反应后的产物 | |
| B. | 甲苯与浓硫酸、浓硝酸60℃加热后生成的有机物 | |
| C. | 苯与液溴、还原铁粉混合后生成的有机物 | |
| D. | 甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个D2O分子中所含中子数为8 | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<HNO3 | D. | 碱性强弱:KOH>NaOH>Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海带中提取碘单质的过程涉及氧化还原反应 | |
| B. | 往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输 | |
| C. | 赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的 | |
| D. | 从海水中获得食盐和淡水必须经过化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
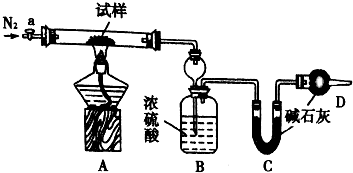 小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如图装置进行实验.| 序号 | a | b | c | d | e |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m3、m5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸与烧碱溶液的反应 | B. | Al与稀盐酸的反应 | ||
| C. | C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO | D. | 葡萄糖在人体内氧化分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸化学式 | CH3COOH | HCN | H2S |
| 电离常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=1.3×10-7K2=7.l×10-15 |
| A. | 等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2S)>pH(NaCN) | |
| B. | CH3COONa溶液中,其水解平衡常数K=Kw×10-5 | |
| C. | NaHS 和 Na2S混合溶液中,存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) | |
| D. | 某浓度NaCN的水溶液pH=d,则其中c(OH-)=10-d mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com