
 国际化学年的中国宣传口号是“化学--我们的生活,我们的未来”.学习化学应该明白“从生活中来,到生活中去”道理.请填空:
国际化学年的中国宣传口号是“化学--我们的生活,我们的未来”.学习化学应该明白“从生活中来,到生活中去”道理.请填空:分析 (1)过氧化钠与水反应生成氢氧化钠和氧气,与二氧化碳反应生成碳酸钠和氧气;
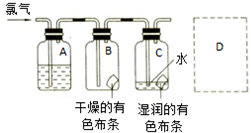
(2)①氯气与水反应生成氯化氢和次氯酸;
②氯气与石灰乳反应生成氯化钙、次氯酸钙和水;
③浓硫酸具有吸水性,干燥的氯气不具有漂白性;
氯气有毒,不能排放在空气中,氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水.
解答 解:(1)过氧化钠与水反应生成氢氧化钠和氧气,与二氧化碳反应生成碳酸钠和氧气,方程式为:2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2
;
2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2
(2)①氯气与水反应生成氯化氢和次氯酸,离子方程式:Cl2+H2O═H++Cl-+HClO;
故答案为:Cl2+H2O═H++Cl-+HClO;
②氯气与石灰乳反应生成氯化钙、次氯酸钙和水,化学方程式:Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
故答案为:Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
③浓硫酸具有吸水性,其作用为吸收气体中的水蒸汽干燥氯气,干燥的氯气不具有漂白性,则与研究目的直接相关的实验现象是B中的布条不褪色,C中的布条褪色,
氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,离子方程式:2OH-+Cl2=ClO-+Cl-+H2O;
故答案为:浓硫酸 吸收氯气中的水蒸气;
点评 本题为实验题,考查了过氧化钠的性质和用途,氯气的制备和性质检验,熟悉相关物质的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Na+、CO32-、OH- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | Mg2+、K+、OH-、Cl- | D. | H+、CO32-、NO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2 L氧气所含的原子数目为NA | |
| B. | 32 g氧气含的原子数目为NA | |
| C. | 5.6 g铁与足量盐酸反应转移的电子数为0.2NA | |
| D. | 2 L 0.1 mol•L-1 K2SO4溶液中离子总数为1.4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维生素不能提供热量,但是对人体有重要作用 | |
| B. | 人体通过生理活动可以合成维生素C,故不需要另外补充 | |
| C. | 维生素C易被氧化,受热易分解,生食富含维生素C的食物可以减少维生素C的损失 | |
| D. | 水果和绿色蔬菜中富含维生素C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | |
| B. | 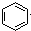 +HNO3$→_{△}^{浓硫酸}$ +HNO3$→_{△}^{浓硫酸}$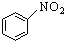 | |
| C. | CH3CH=CH2+B2r→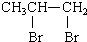 | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com