
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式____________________ 。
(2)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中,P元素的化合价为 _____________。
②NaH2PO2为________(填 “正盐”或“酸式盐”),其溶液显______(填“弱酸性”、 “中性”或“弱碱性”)。
③利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产 物为_____(填化学式)。
【答案】H3PO2![]() H++ H2PO2—+1正盐弱碱性PO43—
H++ H2PO2—+1正盐弱碱性PO43—
【解析】
(1)H3PO2是一元中强酸,溶液中部分电离出氢离子,所以其电离方程式为:H3PO2![]() H++ H2PO2—,故答案为:H3PO2
H++ H2PO2—,故答案为:H3PO2![]() H++ H2PO2—;
H++ H2PO2—;
(2)①由化合物中正负化合价的代数和为零可知H3PO2中,P元素的化合价为+1价,故答案为:+1;②因H3PO2是一元中强酸,故NaH2PO为正盐,属于强碱弱酸盐,由盐类水解可知其水溶液显碱性,故答案为:正盐、弱碱性;③该反应中Ag+为氧化剂,H3PO2为还原剂,氧化剂与还原剂的物质的量之比为4:1,设反应产物中P的化合价为x,根据化合价升降相等可得,4×(1-0)=1×(x-1),解得x=5,所以氧化产物为+5价的H3PO4,故答案为:PO43—(或H3PO4)。


科目:高中化学 来源: 题型:
【题目】有以下一系列反应,最终产物为草酸。
A ![]() B
B![]() C
C![]() D
D![]() E
E ![]() F
F
![]() HOOC-COOH
HOOC-COOH
(1)已知B的相对分子质量比A的大79(已知Br的相对原子质量为80),请推测用字母代表的化合物的结构简式:C是_____________,F是______________ 。
(2)请判断以上各步反应类型
A→B: ______________ B→C:_____________
C→D:___________ E→F:________________________
(3)完成下列反应化学方程式
B→C:___________________________________
D→E:___________________________________
E→F:_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)用水吸收NOx的相关热化学方程式如下:
2NO2(g)+H2O(l)![]() HNO3(aq)+HNO2(aq) ΔH=116.1 kJ·mol1
HNO3(aq)+HNO2(aq) ΔH=116.1 kJ·mol1
3HNO2(aq)![]() HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol1
HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol1
反应3NO2(g)+H2O(l)![]() 2HNO3(aq)+NO(g)的ΔH=___________kJ·mol1。
2HNO3(aq)+NO(g)的ΔH=___________kJ·mol1。
(2)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:____________________________________。
(3)用酸性(NH2)2CO水溶液吸收NOx,吸收过程中存在HNO2与(NH2)2CO生成N2和CO2的反应。写出该反应的化学方程式:____________________________________。
(4)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成1 mol N2时,转移的电子数为__________mol。
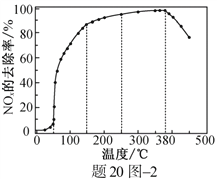
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(装置见题20图1)。

反应相同时间NOx的去除率随反应温度的变化曲线如题20图2所示,在50~250 ℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是____________________________;当反应温度高于380 ℃时,NOx的去除率迅速下降的原因可能是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体能表明②中木炭与浓硝酸发生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,不一定说明木炭与浓硝酸发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是 ( )

A. 正极反应中有CO2生成
B. 微生物促进了反应中电子的转移
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2===6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学是一门以实验为基础的学科,化学实验是化学学习的重要内容。根据掌握的知识判断,下列有关实验操作的描述正确的是________(填下列各项序号)。
A.从试剂瓶中取出的任何药品,若有剩余均不能再放回原试剂瓶中
B.用稀盐酸洗涤盛放过石灰水的试剂瓶
C.配制硫酸溶液时,可先在量筒中加入一定体积的水,再慢慢加入浓硫酸并不断搅拌
D.各放一张质量相同的滤纸于托盘天平的两托盘上,将NaOH固体放在左盘纸上称量
E.NaOH溶液不能保存在带有玻璃塞的试剂瓶中
F.将用水润湿的pH试纸浸入稀盐酸中,测定溶液的pH
(2)化学实验中,不正确的操作会对实验结果的准确性造成一定的影响,请用“>”、“<”或“=”填写下列空白:
①用托盘天平称取10.4 g氯化钠,若将砝码和氯化钠的位置放颠倒了,所称取的氯化钠的质量________10.4 g。
②用容量瓶配制500 mL 0.1 mol·L-1NaOH溶液,定容时仰视刻度线,所得溶液的物质的量浓度________0.1 mol·L-1。
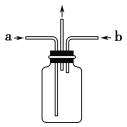
(3)实验时为使氯气、氨气在如图所示装置中充分混合并反应,在a口通入的气体是_______,若氨气量较多,则瓶内会出现大量白烟,该白烟为___________,反应的方程式为___________(已知氮元素被氧化生成常见的单质)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是氯化钠、氯化铵和碳酸氢钠三种物质的溶解度曲线,分析曲线得到的以下说法中,正确的是( )
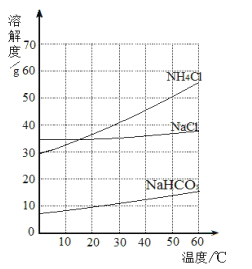
①冷却含有Na+、Cl-、NH4+、HCO3-的浓热的溶液,可得到碳酸氢钠晶体
②在20℃时,三种物质饱和溶液的溶质质量分数为NH4Cl>NaCl>NaHCO3
③在30℃时,氯化钠和氯化铵固体各20g分别溶于50g水,所得溶液都是饱和溶液
④利用结晶法从氯化钠、氯化铵混合物中分离出氯化铵的最佳温度在10℃以下
A. ①②③ B. ①②④ C. ②③④ D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。
(1)基态钴原子的核外电子排布式为___________。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为_____________。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属_____________分子(选填“极性”“非极性”),其立体构型为_____________。
(3)橙红色晶体羰基钴[Co2(CO)8]的熔点为52℃,可溶于多数有机溶剂。该晶体属于_____________晶体。
(4)元素铁、钴、镍并称铁系元素,性质具有相似性。某含镍化合物结构如图所示,分子内的作用力不可能含有_____________(填序号)。
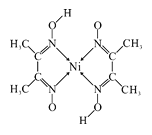
A离子键 B共价键 C金属键 D配位键 E氢键
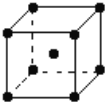
(5)钨为熔点最高的金属,硬度极大,其晶胞结构如图所示,已知钨的摩尔质量为M g/mol,钨原子的半径为a pm。则钨的密度为ρ=_____________g·cm-3。(只需列出计算式,不需化简)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com