


科目:高中化学 来源: 题型:
| A、pH=8的溶液一定显碱性 |
| B、某反应,其他条件不变,升高温度使化学平衡常数(K)增大,则此反应为放热反应 |
| C、相同物质的量浓度的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,则c(NH4+)由大到小的顺序是:①>②>③ |
| D、0.1 mol.L-1 的碳酸钠溶液中:c(OH-)=c(H+)-c(HCO3-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
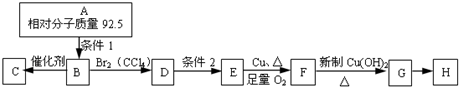
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、镁 | B、铝 | C、锌 | D、铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、塑料奶瓶比玻璃奶瓶更有利于健康,且更加经久耐用 |
| B、“绿色化学”的核心是利用化学原理,解决和治理环境污染问题 |
| C、硅燃烧放出的热量多,且燃烧产物对环境污染程度低,可做“未来石油” |
| D、秸秆的综合利用,如发酵制沼气、生产乙醇等,工艺复杂,还不如一把火烧光还田来得方便 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、都正确 | B、只有①② |
| C、只有①③ | D、只有②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 T/K | 323 | 313 | 303 |
| NO生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com