
【题目】在100℃时,体积不变的密闭容器中发生如下反应:A(g) ![]() 2B(g) ΔH>0,每隔一定时间对该容器内的物质进行分析,得到如下表格,试填空:
2B(g) ΔH>0,每隔一定时间对该容器内的物质进行分析,得到如下表格,试填空:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(A)(mol/L) | 0.100 | c1 | 0.050 | c3 | c4 | c5 |
c(B) (mol/L) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)达到平衡时A的转化率为________。在此条件下,平衡常数K为______。
(2)在0~60s时间段内,A的平均反应速率为_________________。
(3)要使平衡向正反应方向移动,可采取的措施______(填序号)。
A、体积不变时增大的A起始浓度 B、升高温度
C、使用催化剂 D、缩小容器体积
【答案】 60% 0.36 0.001 molL-1s-1 B
【解析】(1)反应的化学方程式为:A(g) ![]() 2B(g),
2B(g),
由表可知,60s时反应达平衡,平衡时c(B)=0.120mol/L,A的起始度为0.1mol/L,则:
A(g) ![]() 2B(g)
2B(g)
起始(mol/L):0.100 0
变化(mol/L):0.060 0.120
平衡(mol/L):0.040 0.120
所以平衡时A的转化率=![]() ×100%=60%,平衡常数K=
×100%=60%,平衡常数K=![]() =
=![]() =0.36,故答案为:60%;0.36;
=0.36,故答案为:60%;0.36;
(2)60s时处于平衡状态,根据①计算可知c3=0.040;由表中数据可知,60s时,v(A)= ![]() =0.001molL-1s-1,故答案为:0.001 molL-1s-1;
=0.001molL-1s-1,故答案为:0.001 molL-1s-1;
(3) A、体积不变时增大的A起始浓度,相当于增大氧气,平衡逆向移动,故A错误;B、升高温度,平衡向吸热的方向移动,平衡向正反应方向移动,故B正确;C、使用催化剂,平衡不移动,故C错误;D、缩小容器体积,压强增大,平衡逆向移动,故D错误;故选B。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
【题目】根据下面各物质之间的转化关系,回答问题:
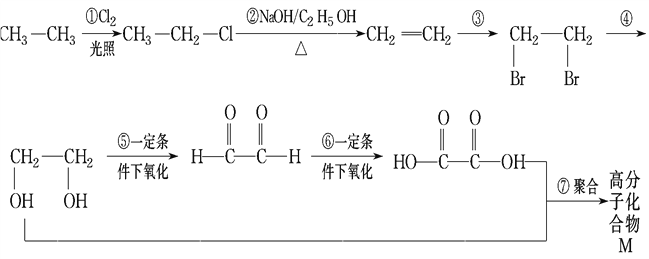
(1)属于取代反应的是___________。
(2)属于加成反应的是___________。
(3)写出反应③、④的化学方程式(有机物用结构简式表示,注明反应条件,下同)
a.反应③___________________________________________________________。
b.反应④__________________________________________________________。
c.写出![]() 和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式 ____________。
和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式 ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】属于道尔顿近代原子论的观点有
A.原子还可由其他更小的微粒构成
B.原子中正电荷是均匀分布在整个原子中
C.原子在化学变化中保持其不可再分性
D.电子在原子核外空间做高速运动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C 又称“抗坏血酸”,在人体内有重要的功能.例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
A.酸性 B.碱性 C.氧化性 D.还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( ) 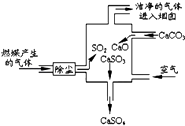
A.此过程中没有分解反应
B.整个过程的反应可表示为:2SO2+2CaCO3+O2═2CaSO4+2CO2
C.使用此废气处理装置可减少CO2的排放
D.此过程中S元素的化合价未发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化盐酸溶液.反应方程式如下:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56L,
计算
(1)参加反应的HCl的物质的量?
(2)反应中被氧化的HCl的物质的量?
(3)并用双线桥标出电子转移的方向和数目.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com